当前位置:APASL-亚太肝脏研究协会年会 » 正文
APASL2019焦点丨NAFLD的治疗进展
—— 作者: 时间:2019-02-25 04:50:24 阅读数:
523

编者按:全球范围内,非酒精性脂肪性肝病(NAFLD)/非酒精性脂肪性肝炎(NASH)是重要的公共卫生问题。对该病的管理必须提上日程。在第28届亚太肝病学会年会(APASL2019)上,我国香港中文大学医学院消化疾病研究所 Vincent Wong教授受邀做State-of-the-Lecture主题演讲,介绍了NAFLD的治疗进展。为帮助未到现场的读者学习,《国际肝病》特将报告内容整理如下。
NAFLD/NASH的现状
全球范围内,非酒精性脂肪性肝病(NAFLD)/非酒精性脂肪性肝炎(NASH)是重要的公共卫生问题,2019年,约累及25%的成人。在美国,NAFLD/NASH已经成为肝移植的第2位适应证,并且是导致肝细胞癌(HCC)的第三大病因。在亚洲,NAFLD/NASH的患病率和严重度稍低,但是,患者的绝对数量最大。NAFLD/NASH可能是多数隐源性肝硬化病例的病因,目前尚无注册的治疗。
非酒精性肝脂肪变(NAFL)又称单纯性脂肪肝,可进展至NASH,发生肝纤维化和肝硬化,最终发生失代偿或HCC,导致患者死亡。期望通过有效治疗,可以阻断NAFLD/NASH的疾病进展,使肝纤维化和肝硬化得到逆转。
应用活性药物对比安慰剂治疗NASH的3期研究的现行要求:基线时,需要对受试者进行肝活检,治疗1-2年时,再次进行肝活检,如果NASH缓解且无肝纤维化加重,或者肝纤维化改善且无NASH加重,则可以得到有条件的批准,之后,需要继续随访患者的长期临床转归(图 1)。
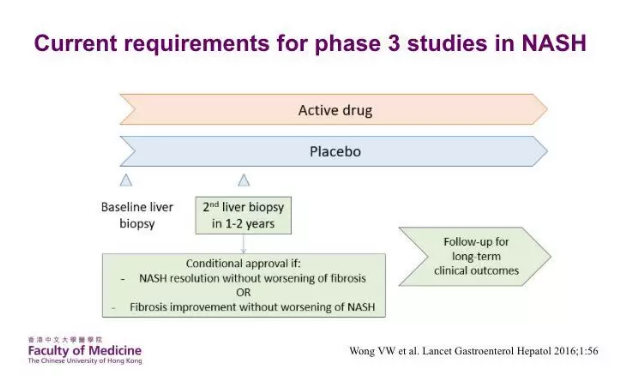
图1. NASH 3期研究的现行要求
亚太NAFLD工作组管理指南建议
根据2017年亚太NAFLD工作组管理指南建议,对NAFL、NASH及其相关肝硬化患者均应进行生活方式干预,如果有指征,可以应用他汀类药物治疗;NAFL患者通常为良性病程,发生肝脏相关并发症的风险较低,而NASH及其相关肝硬化患者则需要药物治疗;对NASH相关肝硬化患者,建议进行食管胃底静脉曲张和HCC的筛查,对HCC发生风险增加的NASH患者,也应该进行HCC的筛查;对病态肥胖患者,建议进行减肥手术治疗。
生活方式干预
健康的生活方式是最重要的NAFLD管理措施,2017年亚太NAFLD工作组管理指南建议的生活方式管理原则:需要多学科团队管理。在限制饮食方面,尚未证实某种饮食明确优于其他饮食;限制饮酒,男性和女性每日酒精饮用量分别应该为<30 g和<20 g;在运动方面,有氧运动和阻力训练均可有效减轻肝脂肪变。
香港一项研究表明,有效的生活方式干预计划可以使NAFLD患者的肝脏脂肪含量显著减少和恢复正常。基于社区的该项随机对照试验纳入144例NAFLD患者,12个月时,19%患者的体重减轻≥10%。体重减轻<3%、3.0-4.9%、5.0-6.9%、7.0-9.9%和≥10%者达到肝内甘油三酯含量低于5%(恢复正常)的比例分别为13%、41%、50%、60%和97%。古巴一项前瞻性研究也证实通过生活方式干预,减轻体重对NASH的治疗效果。该项研究纳入293例经肝活检证实为NASH的患者,1年时,10%的患者体重减轻≥10%。成对肝活检表明,体重减轻<5%、5-7%、7-10%和≥10%者达到NASH消退的比例分别为10%、26%、64%和90%,达到肝纤维化消退的比例分别为16%、18%、16%和45%。
大约10-20%的NAFLD患者为非肥胖人群,香港一项基于社区的研究表明,生活方式干预对肥胖[基线时的体质指数(BMI)>25 kg/m2]和非肥胖(基线时的BMI<25 kg/m2)的NAFLD患者均有效。该项研究总共纳入154例NAFLD患者,随机分组至生活方式干预组(77例)和对照组(77例),基线时每组分别有39例非肥胖患者和38例肥胖患者。无论患者是否肥胖,12个月时,生活方式干预组均有更多患者达到NAFLD消退,其中,非肥胖患者体重减轻<3%、3-5%、5-7%、7-10%和≥10%者达到NAFLD消退的比例分别为14%、50%、60%、75%和100%,肥胖患者体重减轻<3%、3-5%、5-7%、7-10%和≥10%者达到NAFLD消退的比例分别为11%、38%、40%、50%和93%。
现有的药物治疗
维生素E
维生素E是一种抗氧化剂,用于治疗NASH的常用剂量为800 IU/d。吡格列酮、维生素E和安慰剂对照用于治疗无糖尿病的NASH(PIVENS)试验表明,96周时,维生素E组和安慰剂组达到主要转归(肝细胞气球样变减轻≥1分,无纤维化加重;NAFLD活动度评分下降≥2分或降至≤3分)的患者比例分别为43%和19%(P=0.001),达到NASH消退的患者比例分别为36%和21%(P=0.05),达到肝纤维化改善的患者比例分别为41%和31%(P=0.24)。美国一项研究纳入经活检证实为NASH伴桥接纤维化或肝硬化的患者,其中90例应用维生素E(800 IU/d)治疗≥2年,与90例倾向性匹配的未服用维生素E的对照组患者相比,可以阻断疾病进展,不需要肝移植的生存率显著升高(78%对比49%,P<0.01),肝脏失代偿发生率显著降低(37%对比62%,P=0.044)。
但是,患者服用大剂量维生素E,有可能增加死亡风险。一项荟萃分析表明,大剂量维生素E试验中,合并的全因死亡风险差异为39/10000人,但是,这些试验纳入了心血管风险较高以及近期心肌梗死的患者,所以,大剂量维生素E治疗可能并非总体死亡率增加的原因。
吡格列酮
过氧化物酶体增生物激活受体(PPAR)-γ激动剂吡格列酮是一种胰岛素增敏剂。上述PIVENS试验表明,无糖尿病的NASH患者应用吡格列酮治疗96周,和安慰剂组相比,可以使脂肪变及小叶炎症显著改善,达到NASH消退的患者比例分别为47%和21%(P=0.001),达到肝纤维化改善的患者比例分别为44%和31%(P=0.12)。
香港一项研究表明,应用噻唑烷二酮类(TZD)药物治疗,还可以使慢性乙肝患者的肝脏相关并发症事件减少。该项研究纳入28999例合并糖尿病的慢性乙肝患者,其中1153例患者应用TZD治疗,中数随访7.1年,3963例(13.7%)患者发生HCC或肝硬化并发症,以应用TZD ≤1限定日剂量(DDD)作为参照,未应用TZD治疗和应用TZD >1 DDD者发生肝脏相关事件的校正风险比分别为1.40(95% CI:1.02-1.91,P=0.036)和0.31(95% CI:0.10-0.98,P=0.047)。
需要注意吡格列酮治疗过程中可能发生的一些潜在问题,诸如体重增加、液体潴留/充血性心力衰竭、骨质流失以及膀胱癌的发生风险增加等。
胰高糖素样肽-1(GLP-1)激动剂
英国一项多中心2期随机双盲对照试验(LEAN研究)表明,应用GLP-1激动剂利拉鲁肽(1.8 mg/d)治疗48周,可以显著改善NASH患者的肝脂肪变和气球样变,并且可能阻断纤维化进展,利拉鲁肽组和安慰剂组达到NASH消退的患者比例分别为39%和9%(P=0.019),利拉鲁肽组的平均体重减轻5.3 kg,而安慰剂组仅减轻0.6 kg。但是,利拉鲁肽应用不便,需要皮下注射,并且有胃肠道副作用。
非头对头的研究表明,应用维生素E、吡格列酮、利拉鲁肽、水飞蓟素等药物治疗,仅能使一小部分患者达到NASH消退和肝纤维化改善,治疗效果均不如通过有效的生活方式干预,使体重减轻≥10%。
研发中的新药
针对NASH的发病机制和治疗靶点,有许多处于研发过程中的新药,具有一定应用前景(图2)。
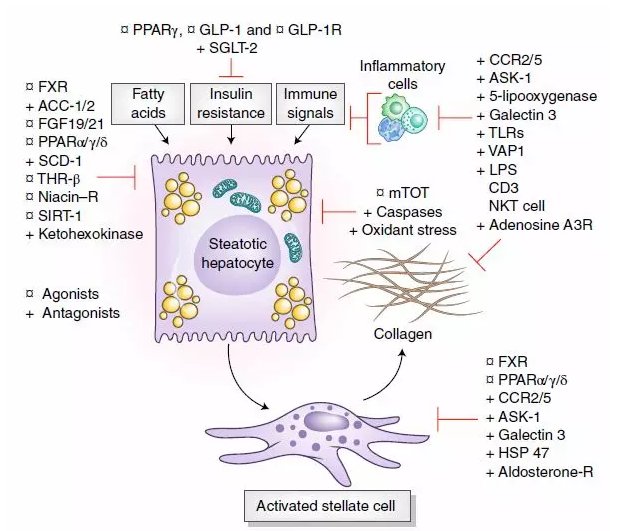
图2. NASH的发病机制和治疗靶点
(摘自Friedman et al. Nat Med 2018;24:908)
奥贝胆酸
奥贝胆酸(OCA)是一种强效的法尼酯受体(FXR)激动剂。美国一项多中心双盲安慰剂对照平行组随机临床试验(2期FLINT研究)表明,应用OCA治疗(25 mg/d)72周,可以改善NASH患者的NAFLD活动度评分、肝脂肪变、小叶炎症、气球样变和肝纤维化,OCA组和安慰剂组达到NASH消退的患者比例分别为22%和13%,达到肝纤维化改善的患者比例分别为35%和19%。研发公司不日前宣布,其III 期临床试验(REGENERATE研究)已经达到了18个月的治疗终点,接受OCA治疗的患者的纤维化消退显著优于对照组。研究结果将在4月召开的欧洲肝病学会(EASL)年会上公布。
OCA治疗的主要不良事件为瘙痒,总胆固醇和低密度脂蛋白胆固醇水平升高,高密度脂蛋白胆固醇水平降低。
PPAR激动剂
PPAR-γ、α和δ对肝脏、脂肪组织、肌肉和血管壁等靶器官或组织具有多种效应。Elafibranor是一种双重PPARα/δ激动剂。欧美一项研究纳入无肝硬化的NASH患者,随机分组至elafibranor 80 mg/d(93例)、120 mg/d(91例)或安慰剂(92例)治疗52周,elafibranor 120 mg/d剂量组与安慰剂组相比,有更高比例的患者达到NASH消退且无肝纤维化加重(19%对比12%,P=0.045)。事后分析表明,elafibranor 120 mg/d对NAFLD活动度评分≥4患者的治疗效果更加显著,并且可以改善胰岛素敏感性和血脂情况。elafibranor 的耐受性良好,10%的患者发生腹痛,血清肌酐值小幅升高。
凋亡信号调节激酶1(ASK1)抑制剂
NASH的进展过程中,发生ASK1通路激活,并且与纤维化分期相关。啮齿类动物模型研究表明,抑制ASK1可以改善肝脂肪变、炎症和纤维化。
GS-4997(selonsertib)是一种强效(EC50:10.8 nM)选择性ASK1小分子抑制剂。美国一项开放标签的多中心2期试验纳入72例2期或3期肝纤维化的NASH患者,随机分组至selonsertib(6 mg/d或18 mg/d)单药治疗、simtuzumab 单药治疗(125 mg,每周注射一次)或selonsertib + simtuzumab联合治疗24周,18 mg selonsertib组、6 mg selonsertib组和simtuzumab单药治疗组达到肝纤维化减轻≥1期的患者比例分别为43%、30%和20%。不过,公司刚刚公布了selonsertib治疗肝硬化(STELLAR-4)患者的12个月结果,显示为阴性,将中止继续研究。而selonsertib治疗F3期患者的STELLAR-3研究还在进行中,结果将会在今年下半年公布。
双重CCR2/5抑制剂
Cenicriviroc(CVC)是一种双重CCR2/5抑制剂,可以阻止枯否细胞激活和巨噬细胞聚集。动物模型研究表明,其具有抗炎和抗纤维化活性,安全性良好。
一项多国随机双盲2b期研究(CENTAUR研究)纳入289例NAFLD活动度评分≥4,肝纤维化1-3期的NASH患者,随机分组至接受CVC(150 mg)或安慰剂治疗1年,CVC组和安慰剂组达到NASH消退且无肝纤维化加重的患者比例相似,分别为8%和6%(P=0.49),然而,CVC组达到肝纤维化改善且无NASH加重的患者比例显著较高(20%对比10%,P = 0.02)。
工程化成纤维细胞生长因子(FGF)
NGM282为工程化FGF19类似物。一项研究表明,NASH患者应用安慰剂、或NGM282(3 mg/d和6 mg/d)治疗12周,肝脏脂肪含量减少≥5%的患者比例分别为7%、74%和79%。另外一项2期研究表明,应用NGM282(3 mg/d)治疗12周,肝纤维化和气球样变得到改善的患者比例分别为42%和53%。
Pegbelfermin(BMS-986036)为聚乙二醇化FGF21类似物。一项研究表明,NASH患者应用10 mg/d和20 mg/周的Pegbelfermin治疗,与应用安慰剂相比,患者肝脏脂肪比例自基线的绝对变化分别为-6.8%、-5.2%和-1.3%(P值分别为0.004和0.008)。
GS-0976(乙酰CoA羧化酶1抑制剂)
应用20 mg/d的GS-0976治疗12周,与安慰剂相比,可以使NASH患者的肝脏脂肪含量显著减少,纤维化生物标志物显著降低,而5 mg/d GS-0976与安慰剂的疗效差异未达到统计学显著性。GS-0976的副作用为高甘油三脂血症,对贝特类治疗有效。
Aramchol
Aramchol是一种脂肪酸-胆汁酸偶联物,可以抑制肝微粒体的硬脂酰CoA去饱和酶-1(SCD-1),而后者是肝脏脂肪生成的一种关键酶,可以将饱和脂肪酸转化为单不饱和脂肪酸。动物模型研究表明,Aramchol可以降低肝脏脂肪酸和胶原蛋白含量。
ARREST试验表明,NASH患者应用安慰剂、Aramchol 400 mg/d或600 mg/d治疗52周,肝脏脂肪含量自基线绝对减少≥5%的患者比例分别为24.4%、36.7%和47%,自基线相对减少≥30%的患者比例分别为14.6%、25.6%和30.1%甲状腺激素受体-β(THR-β)激动剂
人体THR-β激动剂可以降低低密度脂蛋白胆固醇和甘油三酯水平,减少肝脏脂肪,进而可能减轻脂毒性和改善NASH,并且不会导致甲亢毒症(THR-α效应)。
一项研究应用THR-β激动剂MGL-3196(80 mg/d)治疗36周,与安慰剂相比,可以减少肝脏脂肪含量,改善血脂和肝酶水平,NASH消退的患者比例分别为27%和6%,肝纤维化也得到改善。另外一项研究应用THR-β激动剂VK2809(10 mg,QOD或QD)治疗12周,可以减少肝脏脂肪含量,改善血脂和肝酶水平。
从这些新药NASH试验,我们可以学到:所提出的机制可能不同于人体发生的情况(许多情况下,不能将其简单归类为代谢、抗炎和抗纤维化);丰余的通路可能会使最初的治疗反应无效;不要忘记心血管安全性;找到合适的人群和标志物;要考虑到安慰剂效应。对NAFLD/NASH患者应该予以个体化治疗:进行生活方式管理,应用代谢、抗炎和抗纤维化治疗药物,改善炎症坏死和肝纤维化。
标签:
循证视点
主题演讲
脂肪肝
发表评论
全部评论