当前位置:APASL-亚太肝脏研究协会年会 » 正文
APASL热评丨牛俊奇教授:新型HBV CAM(GST-HG141)具有良好的体内外抗病毒活性
—— 作者: 时间:2021-03-16 04:23:53 阅读数:
281

近期乙肝病毒核心蛋白调节剂(HBV CAM)已经成为了有望治疗甚至治愈乙肝病毒的一类新化合物,且已经获得了一定的疗效确证。2021年亚太肝病研究学会(APASL)年会期间,一项题为In Vitro and In Vivo Antiviral Properties of GST-HG141, a Novel Hepatitis B Virus Capsid Assembly Modulator in Clinical Development的摘要入选了大会壁报展示(摘要编号:H-53),该研究报道了一种创新的HBV CAM,即 GST-HG141的临床前数据,其研发目前已处于I期临床阶段。《国际肝病》特邀吉林大学第一医院牛俊奇教授对该研究进行点评。
研究概述
研究方法:
该研究通过 qPCR 技术检测HBV细胞模型的细胞上清中 HBV DNA 含量,测定 GST-HG141 对 HBV 的抑制效果。此外,通过荧光淬灭试验,评价其对HBV 核衣壳组装的抑制活性。雄性 C57BL/6 小鼠通过注射AAV/HBV (D型) 质粒 DNA后建成AAV-HBV小鼠模型以考察体内抗病毒疗效。不同组模型小鼠经28天分别灌胃给予安慰剂 (BID),GST-HG141 (BID),或者替诺福韦酯TDF (QD)。利用real-time qPCR测定血清中HBV DNA 和HBV RNA,同时测定肝脏中HBV DNA。
研究结果:
结果显示,GST-HG141 明显抑制HepG2.2.15细胞中的 HBV DNA ,其 EC50 值为8.16±3.65 nmol/L (表 1)。HepG2瞬时转染细胞的试验表明 GST-HG141 对A、B、C 和 D 型 HBV 均有抗病毒活性 (EC50 26-228 nM, 表 2), 且可以抑制已对核苷(酸)类似物耐药的突变病毒株(表 3)。在11种哺乳动物细胞和原代细胞中未见显著的细胞毒性 (对于MRC-5, HEK293, Caki-1, HepG2, MT-4, Colo-205, H1 HeLa, A375, Hep2 和Huh7细胞系, CC50>50 μM ;对CCRF-CEM细胞 CC50 值为 38 mmol/L)。
表1.GST-HG141及参比药物GLS4(CAM)和替诺福韦在HepG.2.2.15细胞中的抗病毒活性和细胞毒性
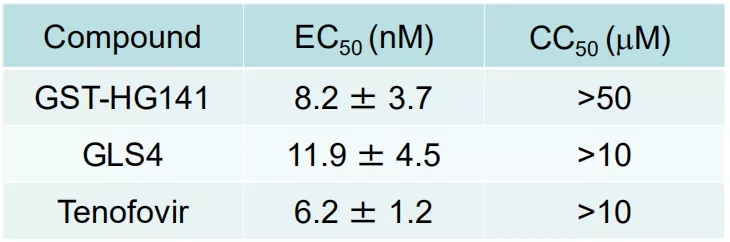
(引自大会摘要H-53)
表2.瞬时转染HepG2细胞对不同基因型分泌型HBV DNA的抑制作用
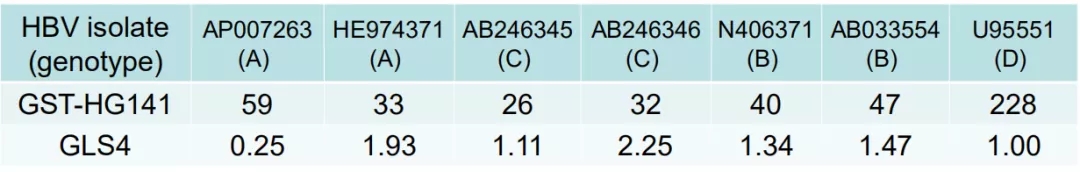
(引自大会摘要H-53)
表3.针对核苷酸(t)耐药突变体的抗病毒活性
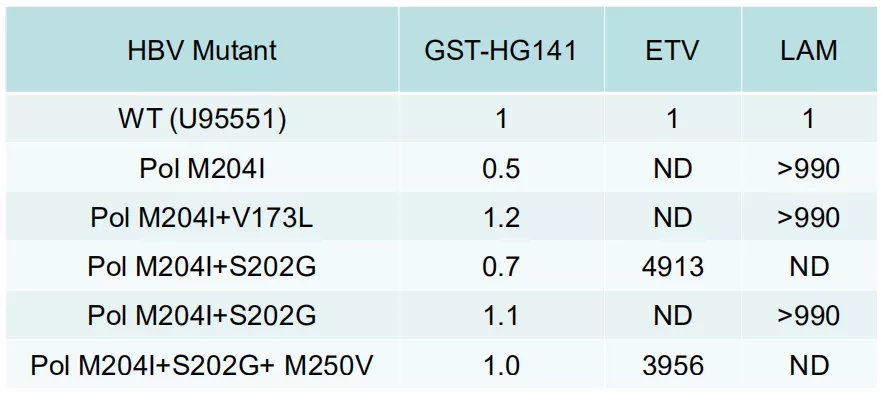
(引自大会摘要H-53)
GST-HG141 抗HBV病毒活性是具有特异性的,因为未见GST-HG141对其他代表性的 DNA和RNA (正负链)病毒有体外抑制作用 (表 4)。 荧光淬灭试验中,发现GST-HG141 抑制HBV 核衣壳蛋白组装, EC50 值为0.93±0.11 μmol/L,该发现与其预期的作用机制吻合,同一试验中GLS4的EC50值为3.34 ± 0.47 μmol/L。
表4.GST-HG141的抗病毒谱
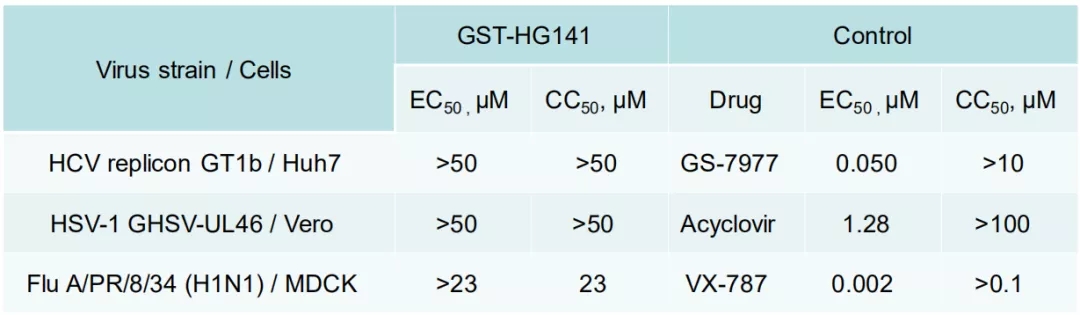
(引自大会摘要H-53)
在AAV/HBV小鼠模型中,GST-HG141 经28天给药后,对血清和肝脏中的HBV DNA拷贝数分别降低了约3.0 log10和0.9 log10,且总体呈现剂量依赖性 (图1) 。在28天给药结束后,乙肝病毒DNA拷贝数快速反弹。GST-HG141对血清HBV RNA水平影响不大,但具有统计学意义。100 mg/kg GST-HG141给予28天后,平均血清 HBV RNA 水平降低了 1.09 log10 GE/mL (在 4.74 ± 0.08到3.64 ± 0.05 log10 GE/ml范围内,P<0.01)。GST-HG141各剂量组在动物模型中均有良好的耐受性,且对体重基本无影响。在连续27天给予 10 mg/kgGST-HG141后,平均GST-HG141谷血浆浓度为78 nmol/L,给药后1小时左右达峰,半衰期为 2.23小时且 AUC0-inf 为47600 nmol/L·h。
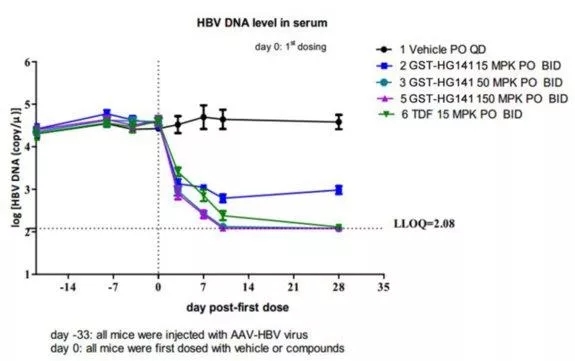
图1.GST-HG141和替诺福韦酯(TDF)对AAV小鼠模型中血清HBV DNA水平的影响
(引自大会摘要H-53)
结论:
GST-HG141是一种新型的口服生物利用型 HBV CAM,其在临床前试验中体现了良好的体内外抗病毒活性,且在啮齿类动物中具有良好的耐受性。以上研究为GST-HG141治疗乙肝方面的进一步开发奠定了基础。目前 GST-HG141正处于I期临床研究阶段。
文献来源:Dong Zhang, Wenqiang Wu, Shikui Chen, et al. In Vitro and In Vivo Antiviral Properties of GST-HG141, a Novel Hepatitis B Virus Capsid Assembly Modulator in Clinical Development. Poster Abstract H-23.
专家点评——牛俊奇教授

乙型肝炎已成为我国重大的公共卫生问题之一,同时也是全世界医学领域共同关注的重要课题。目前,乙肝基本上还不能彻底治愈,大多数患者需要进行长期治疗。
各大公司纷纷积极投入研发能实现功能性治愈乙肝的新疗法中,即实现持久的HBV DNA和表面抗原抑制。包括新靶点的抗病毒药物和免疫调节靶点药物,其中核心蛋白调节剂成为了众多公司着重研发的热点,因为从乙肝病毒的生活史来看,其在抑制乙肝病毒的复制方面相对现有的核苷类药物有着多种的优势。
GST-HG141是一种创新的口服乙肝病毒核心蛋白调节剂,其现已完成临床前体内及体外的药效学研究,药动学研究以及毒理学研究。本期关于GST-HG141的这项研究也入选了2021APASL会议的壁报展示,该研究介绍了GST-HG141的临床前研究成果。
体外研究表明,该化合物能有效抑制乙肝病毒的复制,HepG2.2.15细胞系下的EC50为8.16±3.65 nmol/L,与以往报道的同机制的GLS4相似。体外研究还表明该化合物对各种基因型(A-D)的乙肝病毒表现出了良好的抑制作用(EC50 26-228 nmol/L)。GST-HG141对3株拉米夫定和2株恩替卡韦耐药的乙肝病毒株的抑制活性表明其对耐药突变型病毒抑制活性与野生型相当,与核苷及核苷酸类药物无交叉耐药性。试验结果支持GST-HG141与核苷及核苷酸类药物联合应用,具有广谱的抗核苷及核苷酸类耐药突变的治疗前景。
体内药效实验结果显示GST-HG141(15~150 mg/kg)在AAV/HBV药效动物模型中,经28天BID给药后表现出了良好的抑制HBV DNA的作用,给药后第3天,血清中乙肝病毒DNA拷贝数就显著下降,且各剂量组之间呈显著的量效关系,与现有的乙肝临床用药替诺福韦联用呈明显的叠加效应。但在28天给药结束后,乙肝病毒DNA拷贝数快速反弹。GST-HG141同时显著抑制了乙肝病毒RNA。
GST-HG141在临床前体外和体外的药效学研究中均显示了很好的抗病毒活性和抑制HBV DNA的药效,且临床前药动学和毒理研究中也显示出良好的药动学特征和安全性。以上临床前研究结果为GST-HG141下一步的临床研发奠定了良好的基础,期待GST-HG141能为未来的乙肝治疗带来新的选择。
(作者:牛俊奇,丁艳华,李萃云)

牛俊奇教授
专家简介

牛俊奇教授
吉林省肝病研究所所长、吉林大学第一医院肝病科主任,临床药理机构教授,《临床肝胆病杂志》主编。承担“十二五”重大专项等多项国家重要研究项目。国家自然科学基金9项。参与肝病临床研究项目共计114项。共发表SCI科研文章141篇,总影响因子584;其中第一作者或通讯作者发表文章70篇,影响因子196。并获得教育部高等院校科研优秀成果奖一等奖1项,中华医学科技奖二等奖1项,吉林省自然科学奖一等奖2项。
(来源:《国际肝病》编辑部)
标签:
述评/点评
名家视点
乙肝
发表评论
全部评论