当前位置:ILCA-世界肝癌学会年会 » 正文
ILCA2020丨周俭教授:叩开晚期肝癌免疫之门的“T+A”开创“免疫+X”新时代
—— 作者: 时间:2021-03-25 03:35:19 阅读数:
5
编者按:随着IMbrave150研究数据在国际顶级期刊《新英格兰医学杂志》的重磅公布,阿替利珠单抗联合贝伐珠单抗(简称“T+A”)在晚期肝癌的疗效突破既往金标准索拉非尼,标志着晚期肝癌一线治疗正式迈入免疫治疗新时代。
2020年9月11~13日,第14届国际肝癌协会年会(ILCA2020)召开期间,我国复旦大学附属中山医院副院长周俭教授应邀进行主题报告,讨论晚期肝癌治疗的格局变化,盘点ESMO、NCCN、AASLD及CNLC四大指南的最新治疗推荐,并借智十余年的临床用药积淀,思考“免疫+X”治疗新格局下的患者最大化获益模式。
晚期肝癌一线系统治疗盘点,MDT助力患者生存延长
肝细胞癌(HCC)是全球第6位最常见恶性肿瘤和第4位肿瘤致死病因。2007年以前,HCC在局部治疗失败后无有效治疗方法,患者预后极差。
2007年SHARP研究的成功,奠定了索拉非尼在晚期HCC治疗中十余年的一线治疗地位[1]。但遗憾的是在随后的十年中,舒尼替尼、布立尼布、利尼伐尼等药物治疗晚期HCC的Ⅲ期研究均以失败告终[2-4]。
2018年RELFECT研究结果宣告,仑伐替尼在与索拉非尼的头对头研究中,以在主要终点OS的非劣效性获得试验的成功,进入晚期HCC的一线治疗(图1)[5]。
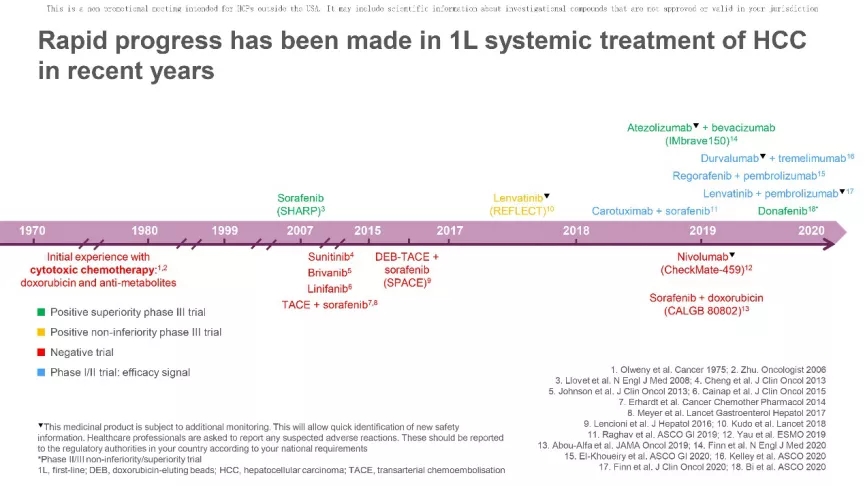
图1.晚期HCC一线系统治疗盘点
(引自ILCA2020报告幻灯)
在近13年的晚期HCC药物研发历程中,仅有索拉非尼和仑伐替尼这两种TKI在全球被批准用于晚期HCC的一线治疗。
细看索拉非尼在晚期HCC临床试验中的生存数据可以发现,从2007年SHARP研究的OS 10.7个月增加到2019年CheckMate-459研究的14.7个月,延长了近4个月[1,6]。可能原因为:
√瑞戈非尼、卡博替尼等晚期HCC二线治疗的成功应用;
√索拉非尼应用经验的提升;
√以外科、胃肠病科、肝病科、肿瘤内科、介入放射科和护士在内组成的多学科团队(MDT)对治疗的最优化制定和个体化选择(图2)。

图2.晚期HCC MDT团队
(引自ILCA2020报告幻灯)
“T+A”突破肝癌晚期一线金标准,为患者带来更长久生存
索拉非尼作为标准疗法治疗晚期HCC已经有十多年的时间,但整体疗效有限,并存在耐药的问题。“T+A”免疫联合疗法给晚期HCC患者带来希望。
在IMbrave150中,与目前的标准治疗索拉非尼相比,“T+A”免疫联合治疗方案显著延长患者OS和PFS。
“T+A”方案使患者死亡风险相对下降了42%[风险比(HR)=0.58;95%CI:0.42~0.79;P=0.0006]。疾病进展风险方面,“T+A”组患者的中位PFS从4.3个月提升到了6.8个月。
而在12个月生存率方面,“T+A”免疫联合治疗组达到67.2%,预计缓解时间超过6个月的患者在“T+A”组占87.6%,远高于索拉非尼组的59.1%[7]。
基于“T+A”在晚期HCC的优秀数据,美国FDA于今年5月批准“T+A”用于晚期不可切除或转移性HCC适应证,也是目前首个可用于晚期HCC的免疫联合疗法。
ESMO指南推荐“T+A”可用于BCLC C期HCC的一线治疗;BCLC B期TACE治疗失败后也可应用“T+A”等系统治疗[8]。
另外三大指南NCCN、AASLD及CNLC也随即跟进,均推荐“T+A”免疫联合治疗为晚期肝癌的一线治疗(图3)[9-11]。
此外,MDT合作在晚期HCC的治疗中也起着举足轻重的作用。

图3.ESMO、NCCN、AASLD及CNLC均一线推荐“T+A”用于晚期HCC
(引自ILCA2020报告幻灯)
“T+A”——me first,占据晚期HCC免疫治疗研发最高点
正是由于“T+A”联合免疫治疗在晚期HCC治疗中的突破性成功,开创并引领了晚期HCC治疗“免疫治疗+X”的新局面。
IMbrave150研究是目前晚期HCC阶段唯一一个成功的Ⅲ期临床试验,也正是由于晚期HCC“T+A”全球“me first”创新疗法,增强了其他“免疫治疗+X”联合疗法成功的信心并提供了宝贵经验(图4)[12]。
相信会有越来越多的“免疫治疗+X”联合疗法,为晚期HCC的治疗添砖加瓦。

图4.“T+A”开创晚期HCC“免疫治疗+X”治疗新局面
(引自ILCA2020报告幻灯)
总结
晚期HCC系统治疗已进入飞速发展的新局面,这得益于IMbrave150研究“T+A”的开拓性治疗。“T+A”也成为目前全球唯一的晚期HCC一线治疗推荐。MDT治疗将助力晚期HCC治疗,使患者获得更长生存。
参考文献:
[1] Tormey DC. Sorafenib in Advanced Hepatocellular Carcinoma[J]. N Engl J Med, 2008, 359(23):378-390.
[2] Cheng AL, Kang YK, Lin DY, et al. Sunitinib Versus Sorafenib in Advanced Hepatocellular Cancer: Results of a Randomized Phase III Trial[J]. Journal of Clinical Oncology, 2013.
[3] Johnson P, Qin S, Park J, et al. Brivanib versus sorafenib as first-line therapy in patients with unresectable, advanced hepatocellular carcinoma: results from the randomized phase III BRISK-FL study.[J]. Journal of Clinical Oncology, 2013, 31(28):3517.
[4] Cainap C, Qin S, Huang WT, et al. Linifanib versus Sorafenib in patients with advanced hepatocellular carcinoma: results of a randomized phase III trial[J]. Journal of Clinical Oncology, 2015, 33(2): 172.
[5] Kudo M, Finn RS, Qin S, et al. Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomized phase 3 non-inferiority trial[J]. The Lancet, 2018, 391(10126): 1163-1173.
[6] Yau T, Park JW, Finn RS, et al. CheckMate 459: A randomized, multi-center phase III study of nivolumab (NIVO) vs sorafenib (SOR) as first-line (1L) treatment in patients (pts) with advanced hepatocellular carcinoma (aHCC)[J]. Annals of Oncology, 2019, 30: v874-v875.
[7] Finn RS, Qin S, Ikeda M, et al. Atezolizumab plus bevacizumab in unresectable hepatocellular carcinoma[J]. New England Journal of Medicine, 2020, 382(20): 1894-1905.
[8] eUpdate – HCC treatment recommendations (June 2020).
[9] NCCN guidelines v4.2020.
[10] Llovet, et al. Hepatology 2020.
[11] CNLC, 2020.
[12] clinicaltrials.gov
(来源:《国际肝病》编辑部)
标签:
新知
肝癌
发表评论
全部评论