当前位置:AASLD-美国肝病研究学会年会 » 正文
AASLD热评丨陈成伟教授:COVID-19期间肝损伤,原发还是继发?——其重要性及相关因素分析
—— 作者: 时间:2021-03-30 05:41:38 阅读数:
16
在COVID-19大流行期间,SARS-CoV-2感染患者常伴随肝酶异常(主要为AST和ALT升高),但我们尚不确定这种肝损伤表现是否源自病毒对肝脏的直接损害。2020年美国肝病研究学会(AASLD)年会期间,美国耶鲁大学医学院Michael Chew等人报告了其对这一问题的研究结果,提示COVID-19相关的肝酶异常主要是继发于其他损伤(摘要编号:LP27),为COVID-19相关肝损伤机制研究提供了新思路。《国际肝病》特邀海军军医大学附属九〇五医院陈成伟教授对该研究进行点评。
研究概述
COVID-19常伴随肝酶异常(主要为AST和ALT升高),尚不确定SARS-CoV-2对肝脏是否有直接损害,是否会导致肝衰竭和死亡;抑或是否是继发性的伴随过程,如缺血、药物性肝损伤、炎性状态和/或高凝状态等。
作者假设观察到的肝损伤可能是继发性事件,且与肝衰竭或较高的死亡率无关。将2020年4月1日至4月30日连续入院的COVID-19的836例患者纳入研究,在入院基线和整个在院期间均作必要的生化等检查,记录临床状况和所用药物。
严重COVID-19定义为使用升压+气管插管;局部缺血定义为使用血管加压药;高度炎症状态定义为CRP>100 mg/dL或铁蛋白>1000 ng/mL;高凝定义为静脉血栓栓塞(VTE)、D-二聚体>5 mg/dL或纤维蛋白原>700 mg/dL 。
结果表明,严重COVID-19患者(n=138)与非严重COVID-19患者相比,入院时AST(52 vs. 37 U/L,P<0.001)和ALT(35 vs. 24 U/L,P<0.001)更高,AST峰值(89 vs. 37 U/L,P<0.001)和ALT峰值(57 vs. 24,P<0.001)也高,白蛋白降低(3.3 vs. 3.6 g/dL,P<0.001),但胆红素(0.56 vs. 0.49 mg/dL,P=0.14)或INR(1.12 vs. 1.05 mg/dL,P=0.18)无差异。
整个住院期间log AST和log ALT的变化显著相关(R=0.89),而log AST的变化与log INR的变化不相关(R=0.10)(图1)。105例AST>5×ULN患者的多因素logistic回归分析显示,缺血(OR 3.9)和托珠单抗的使用(OR 3.5)是独立预测因子,而与高凝和炎症反应无关。138例(16.5%)患者死亡多因素Logistic回归分析显示缺血与死亡独立相关(OR 3.4),而AST>5×ULN则不相关(OR 1.4)。
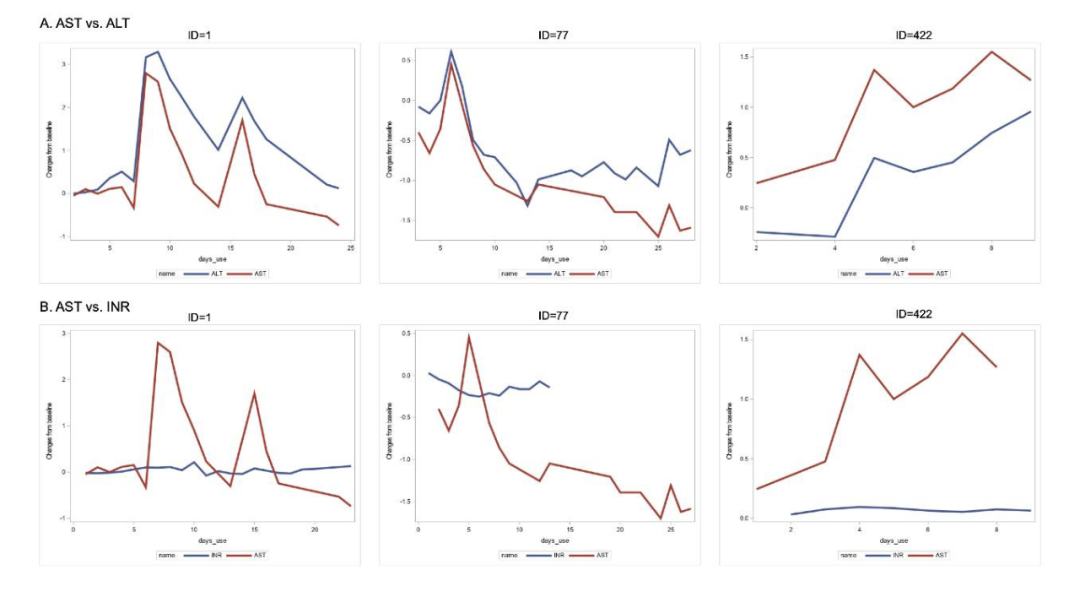
图1.AST、ALT和INR变化比较
因此作者认为,COVID-19相关的肝酶异常主要是继发于其他损伤(如局部缺血或药物引起的肝损伤),并不会导致肝功能衰竭或死亡。
点评
在COVID-19发生、发展及治疗和过程中出现的相关生化学检查明显异常,即ALT或AST>3×ULN,或总胆红素>2×ULN。
今年疫情以来,众多研究对其发生机制进行了报道。早在今年3月下旬,中国医师协会消化医师分会和中华医学会肝病学分会就发布了《新型冠状病毒肺炎合并肝脏损伤的预防及诊疗方案》。究其原因,不外乎以下几个。
其一,为病毒的直接毒性作用,依据为病理表明肝大,肝细胞变性、灶状坏死伴中性粒细胞浸润,肝血窦充血,汇管区淋巴细胞和单核细胞浸润。
其二,为微血栓形成所致的应激与全身炎症反应,部分COVID-19患者发病早期临床表现较轻,但发病1周左右突然加重,甚至很快进入MODS再到MOF状态,很可能是由于免疫细胞释放大量TNF、IL-6、IL-18等炎症细胞因子,导致 SIRS和ARDS,并诱发机体缺氧,进一步导致更多细胞损伤、坏死。
其三,为COVID-19所致的肝脏缺血和低氧,COVID-19患者存在不同程度低氧血症,其中近半数需要给予氧疗。因此,缺血和低氧很可能是重型和危重型COVID-19患者出现肝损伤的主要机制之一。
其四,为基础肝脏疾病加重,慢性乙型肝炎、慢性丙型肝炎、酒精性肝病、非酒精性脂肪性肝病、自身免疫性肝病等基础肝病,有可能在COVID-19时加重。
其五,也是很重要的就是药物性肝损伤,特别要注意的是,重型患者常接受多种药物治疗,有报道超过50%的接受抗生素静脉用药,45%接受2种以上抗生素联合治疗,持续时间3~17天。因此,药物性肝损伤决不能忽视,在COVID-19临床治疗上应引起高度重视。
本研究结果表明COVID-19相关的肝酶异常主要是继发于其他损伤,并不会导致肝功能衰竭或死亡。为COVID-19相关肝损伤的机制研究提供了一个很好思路。不过,这是一个单中心的回顾性研究,循证证据的级别尚不够高。
(来源:《国际肝病》编辑部)
标签:
新知
其他肝病
发表评论
全部评论