当前位置:APASL-亚太肝脏研究协会年会 » 正文
APASL2022丨廖家杰教授:COVID-19相关肝损伤的诊治与挑战
—— 作者: 时间:2022-04-01 10:02:51 阅读数:
62
3月30日至4月3日,第31届亚太肝病研究学会(APASL)年会在韩国首尔如期召开。国内外领域专家学者线上线下互联,共襄此次盛会。会上,中国香港天下仁心医疗集团主席、北京解放军总医院第五医学中心(原解放军第302医院)联合香港天下仁心医疗集团肝病与移植中心共同主任廖家杰教授进行了关于“Spectrum and management of COVID in ACLF”的主题报告。《国际肝病》特将报告整理如下,以飨读者。
目前已知,COVID-19感染不仅导致肺部的炎性损伤(新冠肺炎),更可引起包括肝脏在内的全身多系统多器官的损伤。因此,自疫情暴发以来,国内外肝病领域专家、学者一直在搜集、分析研究COVID-19患者的肝损伤情况,特别是慢性肝病(CLD)患者在COVID-19感染后出现的肝损伤,目前相关数据、经验不断积累更新,以期更好地指导临床诊疗。
2020年下半年,APASL COVID肝损伤研究组在Hepatol Int杂志发表的一篇论文[1]指出,感染前罹患肝脏疾病与不良预后有关,五分之一的肝硬化患者出现肝功能失代偿(图1)。数据显示,已经出现失代偿的患者,其临床状况可能进一步恶化,肝损伤的严重程度与COVID-19的严重程度相关;潜在慢性肝病的存在可能使COVID-19患者发生严重肝损伤的风险更高,如慢加急性肝功能衰竭;此外伴有糖尿病和肥胖症的慢性肝病患者,其肝脏更容易受到损伤,因此应密切监测。
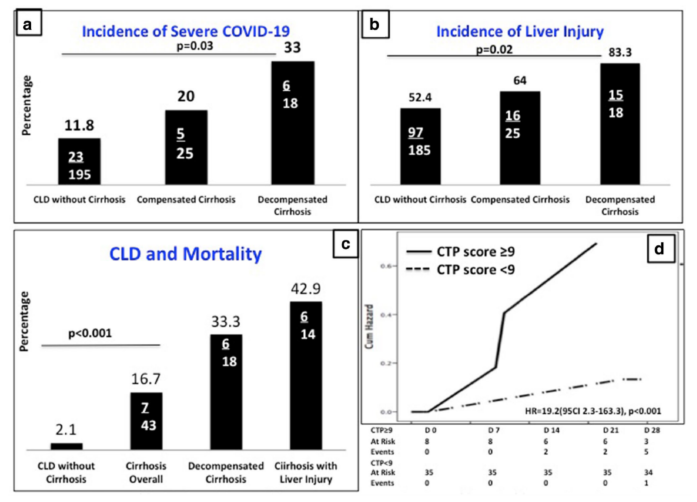
图1. COVID-19与慢性肝病的不良预后
(引自发表文章)
另一项国际注册研究[2]数据显示,基线肝病分期和酒精相关性肝病是新冠肺炎死亡的独立危险因素,晚期肝硬化患者的死亡风险高于无肝病倾向评分匹配对照组,而肝硬化死亡患者中大多数是死于由COVID-19感染导致的相关肺病。这些数据对于新冠肺炎疫情期间全球CLD患者的风险分层具有重要意义。
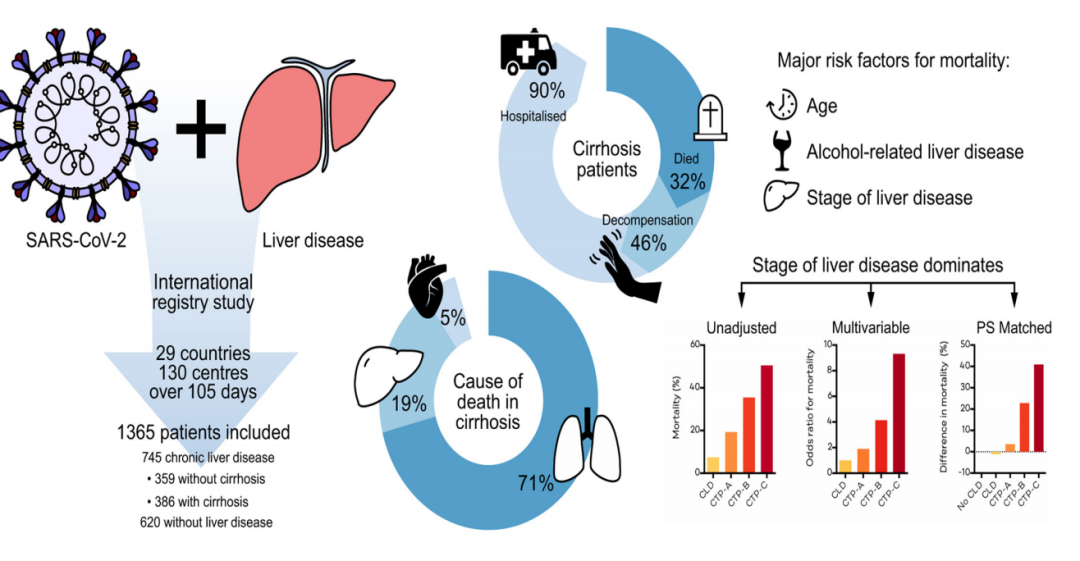
图2. 国际注册研究方案与数据
(引自讲者报告)
数据显示,COVID-19患者的肝损伤以肝细胞损伤为主,而非胆汁淤积性,同时伴有肝细胞变性、局灶性坏死、毛细胆管胆汁淤积及门脉区炎症。目前,COVID-19相关肝损伤的潜在机制尚不明确。专家提出可能的机制包括:病毒感染直接引起肝细胞损伤、免疫失衡和细胞因子风暴相关的多器官损伤以及因COVID-19感染使用的各种药物引起的药物性肝损伤。此外,COVID-19相关并发症(如呼吸窘迫综合征、全身炎症反应综合征、多器官衰竭等)引起的缺氧和休克也可能导致肝脏缺血缺氧再灌注损伤。
关于COVID-19感染的治疗,目前尚缺乏明确有效的抗病毒药物,针对病因治疗在现阶段还是难以企及。因此,世界各地的科学家正在努力研究COVID-19的潜在治疗方法(图3)。
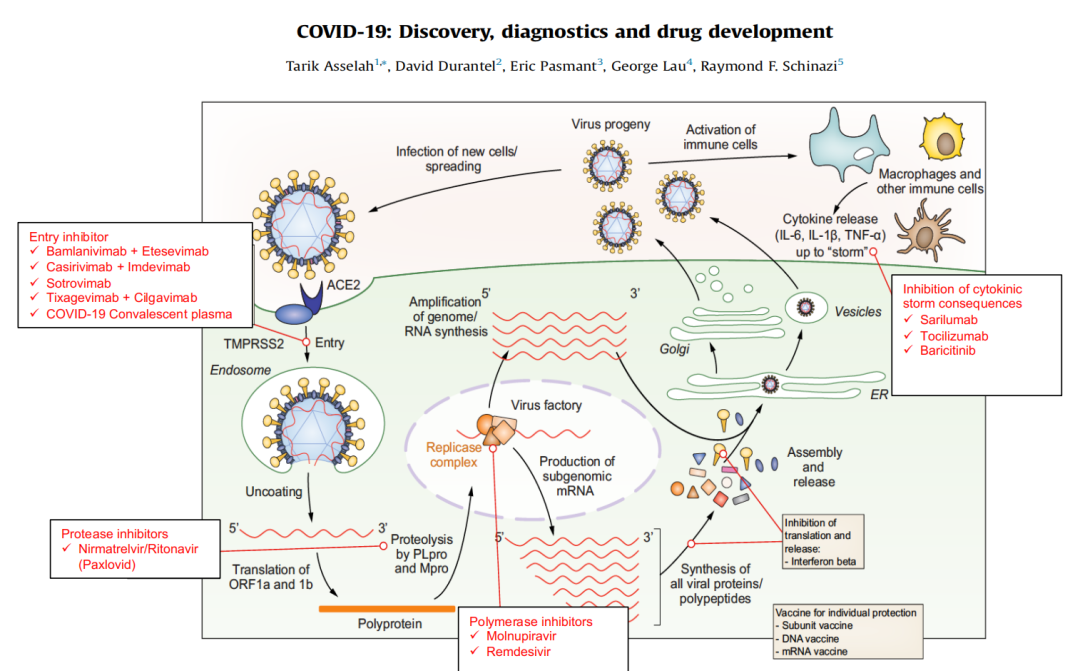
图3. COVID-19药物靶点[3]
(引自发表文章)
抗病毒药物
目前美国FDA相继批准了辉瑞的Paxlovid和默沙东的Molnupiravir 两种口服抗病毒药物的紧急使用授权申请。Paxlovid是由Nirmatrelvir(一种病毒蛋白酶抑制剂)与Ritonavir(利托那韦,CYP3A抑制剂)组成的复方制剂,适用于未接种疫苗的轻至中度COVID-19成年患者,可将高危患者的住院率或全因死亡率大幅降低近90%。目前尚缺乏关于Nirmatrelvir/Ritonavir在严重肝损伤(Child-Pugh C)患者中的药代动力学或安全性数据。但既往有数据显示,接受利托那韦治疗的患者出现过伴有转氨酶升高的肝损伤、肝炎和黄疸。因此,对于已有肝脏疾病、肝酶异常或肝炎的患者,在使用Nirmatrelvir/Ritonavir时应谨慎;瑞德西韦和Nirmatrelvir/Ritonavir不推荐用于丙氨酸转氨酶高于正常上限5倍或肝脏失代偿的患者;在使用瑞德西韦治疗的患者中,已经有肝功能紊乱导致停药的报道。
另一种抗病毒药物Molnupiravir,是一种核苷类似物,可诱导SARS-CoV-2基因组发生致命突变,可将患者住院率或全因死亡率降低约30%。

图4. COVID-19抗病毒药物
(引自讲者报告幻灯)
免疫调节药物
白介素6(IL-6)是COVID-19患者中升高的细胞因子,目前IL-6抑制剂(托珠单抗,Sarilumab)已用于治疗伴有IL-6水平升高的严重肺损伤患者。但这种药物有导致重度感染的“黑框”警告,包括乙型肝炎病毒(HBV)再激活导致暴发性肝衰竭。因此,对于HBsAg阳性的COVID-19患者,需要服用抗HBV药物以防止再激活的发生。
此外,有报道表明,传统中药的使用也可能导致急性肝衰竭,甚至需要肝移植。

图5. COVID-19免疫调节药物
(引自讲者报告幻灯)
可喜的是,基于最新研究数据,由亚太地区16个国家/区域的肝病学家组成的工作小组已经发布了亚太肝病学会COVID-19专家组共识建议[4],以期在COVID-19大流行期间为肝病和肝移植医务人员提供临床实践指导。
参考文献
1. Sarin SK, Sharma M, Lau G et al. Hepatol Int. 2020;14(5):690-700.
2. Marjot T, et al. J Hepatol. 2021;74(3):567-577.
3. Asselah T, et al. J Hepatol. 2021 Jan;74(1):168-184 (modified).
4. APASL Covid-19 Task Force, Lau G, Sharma M. Hepatol Int. 2020 Jul;14(4):415-428.
标签:
访谈
热点聚焦
其他肝病
发表评论
全部评论