当前位置:APASL-亚太肝脏研究协会年会 » 正文
APASL重磅|贾继东教授:初战告捷——siRNA疗法BRII-835(VIR-2218)治疗慢乙肝II期临床试验显示安全有效
—— 作者: 时间:2022-04-07 10:47:34 阅读数:
438
编者按
2022年4月3日,第31届亚太肝脏研究学会(APASL)年会圆满结束。期间,首都医科大学北京友谊医院贾继东教授牵头的一项利用小干扰核糖核酸(siRNA)BRII-835(VIR-2218)治疗慢性乙型肝炎(CHB)的II期临床试验获得重要进展,被大会收录为Late-Breaking Abstract(大会摘要号:L-OP-1324),贾继东教授在大会上做了视频发言,引起了广泛关注。本刊特邀请贾继东教授为我们详细讲解有关BRII-835(VIR-2218)的独特作用机制,分享该项研究结果的临床意义。
《国际肝病》您在本届大会中报告了一项应用siRNA技术(BRII-835)治疗慢乙肝的临床研究,BRII-835抗HBV的作用机制是什么?
贾继东教授:BRII-835是一种研究性的siRNA疗法,它靶向的是乙型肝炎病毒(HBV)的X基因。理论上,如果把HBV的X基因阻断,那么对HBV其他的基因都有一定的阻断作用,从而抑制了HBV抗原的表达,临床上能够降低病毒抗原的负荷,尤其是HBsAg的负荷——这也是国际上CHB治疗实现功能性治愈的主要考察指标。
关于沉默基因的这个靶点,目前国际上各大制药公司所采用的技术策略以及具体一些细节各不相同,但基本作用原理都是直接干扰HBV基因的表达,使其不能产生包括HBsAg在内的多种的抗原成分。所以,这也是siRNA疗法有望作为治愈CHB药物之一的主要原因。
《国际肝病》如此说来,BRII-835可以沉默全部乙肝病毒RNA转录物,甚至包括cccDNA。请您结合这个话题谈谈该项技术相比其他乙肝治疗路程路径的独特优势?
贾继东教授:关于CHB的抗病毒治疗,目前国际上研发了很多针对HBV复制周期或者生命周期不同靶点的药物,其中之一就是siRNA疗法,可以干扰病毒RNA的表达,影响病毒颗粒的组装。理论上,这是有可能把HBV逐渐清除的一条途径。不过,慢性HBV感染是一个非常复杂的过程,除了在肝细胞内存在共价闭合环状DNA(cccDNA)以外,在感染者的基因组里中也可能存在整合的病毒DNA。因此,我们说CHB的治疗是非常困难的。单独通过siRNA疗法能否彻底治愈CHB目前还不能确定,但有可能与其他抗病毒药物形成联合疗法。
在我们的这项II期临床试验中,选择的是经口服核苷(酸)类似物(NA)治疗半年以上,且HBV DNA水平降低到一定水平,转氨酶水平也比较低的CHB患者。在这些患者中,我们希望能够通过siRNA疗法,在病毒抑制的基础上继续把HBsAg水平降低,从而实现HBsAg的转阴,也就是CHB的临床治愈。
《国际肝病》请您为我们介绍一下在本届APASL大会上您报告的关于BRII-835的最新研究进展?
贾继东教授:这是一项在中国CHB患者中进行的II期随机、双盲、安慰剂对照试验。既往的研究表明,在CHB患者中,BRII-835(每月一剂20~200 mg,共两剂)的耐受性良好,在所有剂量水平的HBeAg阳性和HBeAg阴性受试者中均观察到HBsAg的显著降低(EASL 2021)。我们在本届APASL年会上展示了BRII-835在中国CHB患者中的安全性和抗病毒活性数据。
研究共纳入21例NA经治、HBV DNA<90 IU/mL和ALT和AST均≤ 2×ULN的CHB患者。所有受试者按4:1的比例,随机接受每隔4周1次BRIl-835(50 mg或100 mg)或安慰剂皮下注射,共两剂。评估包括第16周对所有受试者在两剂给药后的安全性和HBsAg水平,并对HBsAg降低≥1 log10 的受试者进行额外32周的随访。
结果显示,BRII-835(VIR-2218)的耐受性良好。没有受试者因不良事件(AE)而停药,所有受试者治疗中出现的不良事件(TEAE)的严重程度均为1级或2级。未观察到有临床意义的ALT升高。
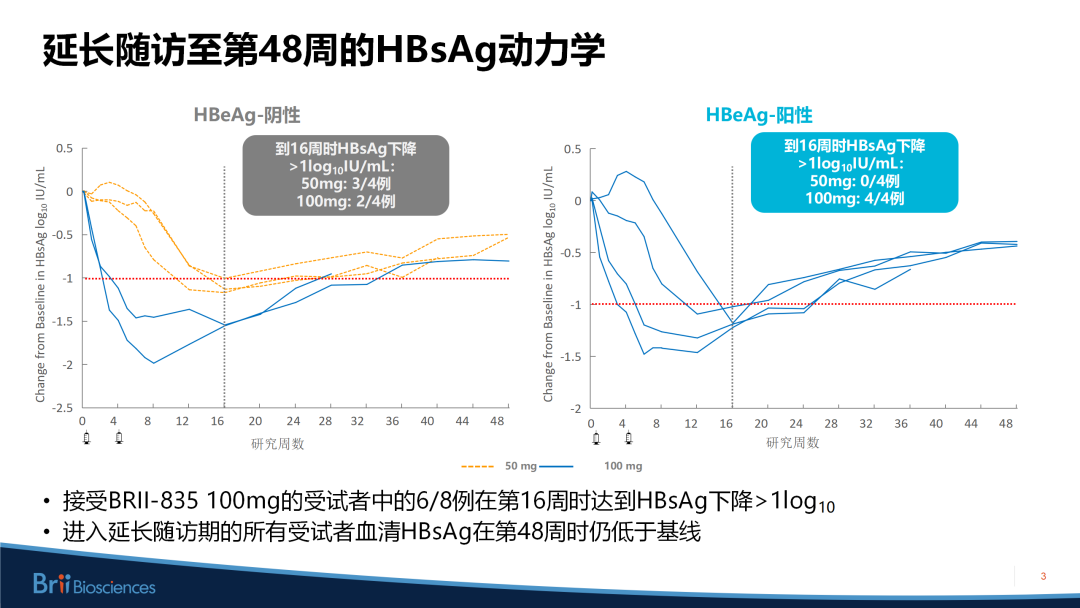
第16周时,接受50 mg和100 mg BRII-835治疗的HBeAg阴性CHB受试者中,HBsAg平均下降了1.02 log10 lU/mL和1.22 log10 lU/mL;相应地,在HBeAg阳性CHB受试者中,分别下降了0.70 log10 lU/mL和1.15 log10 lU/mL。除此之外,75%接受100 mg BRII-835的受试者,末次给药后12周HBsAg下降>1 log10 IU/mL,且至第48周时血清HBsAg水平始终低于基线水平。
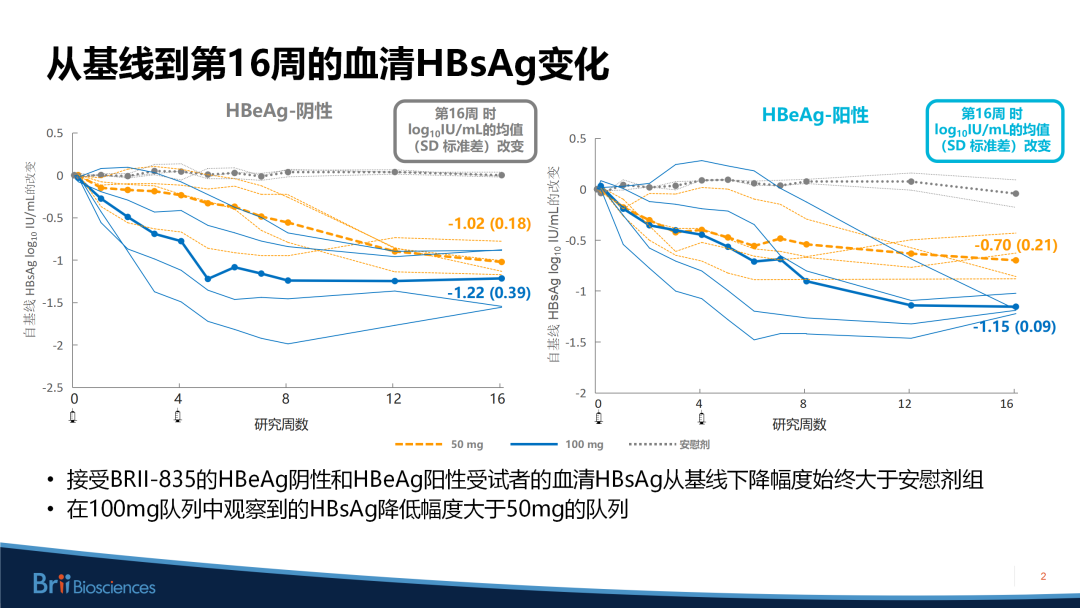
该项研究结果表明,中国慢性乙型肝炎患者对于50 mg、100 mg BRII-835的耐受性良好,HBeAg阴性和HBeAg阳性CHB患者的血清HBsAg水平均有剂量依赖性显著降低,与之前的研究结果一致。
《国际肝病》除此之外,我们是否比较分析过其他病毒学应答指标,比如HBV DNA水平的变化,甚至可能的话,更为直观地比较受试者肝细胞内cccDNA水平的变化?
贾继东教授:所有受试者在入组前经过NA治疗后,HBV DNA水平已经降到很低了(HBV DNA<90 IU/mL),因此我们不再把它作为该项研究的主要观察指标,而是把HBsAg——这个最难实现的指标作为一个观察重点。至于cccDNA水平,因需要进行组织学的检查而未进行。但是我们可以从一些间接性的指标,例如HBV RNA和核心相关抗原(HBcrAg)来反映药物对cccDNA和整合DNA转录的抑制。如前所述,在我们这项研究中,接受BRII-835治疗的受试者,血清HBsAg水平均显著降低;在第16周HBsAg下降>1 log10 IU/mL的所有受试者,血清HBsAg能够在随访的48周内一直保持在低于基线以下。这提示药物可降低来自cccDNA和整合DNA的转录产物。

《国际肝病》请您谈谈该项研究成果具有怎样的临床意义?以及接下来针对BRII-835,我们还将开展哪些研究工作?
贾继东教授:我们的这项研究是一项II期临床试验,也是早期的探索。除了看到了BRII-835初步的效果,我们也在摸索合适的给药剂量。目前,我们已经初步看到BRII-835 50 mg、100 mg都有降低HBsAg的作用,并且HBsAg水平呈剂量依赖性降低。这些数据提示,BRII-835具有治愈CHB的潜力,为BRII-835联合其他不同靶点的药物提供了广阔前景。
未来,关于BRII-835的进一步研究还有很多值得探讨的问题,例如是否进一步延长疗程,如何与其他药物联合等等。归根结底,我们的最终目标不仅仅是HBsAg单纯的下降,而是HBsAg能够转阴,即实现CHB临床治愈这一最终目标。
标签:
访谈
名家视点
乙肝
发表评论
全部评论
