
编者按
2024年11月15日~19日,美国肝病研究学会年会(AASLD 2024)于美国圣迭戈举行。首都医科大学附属北京佑安医院肝病消化中心丁惠国教授团队的研究成果被大会收录,并荣获大会优秀壁报(Poster of Distinction)。该课题主要由刘燕娜博士和何杨兰(在读博士研究生)完成,刘燕娜博士获得“2024 Interational Early Career Investigator Award”。

刘燕娜博士在AASLD 2024会议现场
研究背景
肝硬化是门静脉高压最常见的病因,但仍有15%~20%的门静脉高压由非硬化原因引起1,特发性非肝硬化性门静脉高压(idiopathic non-cirrhotic portal hypertension,INCPH)是其中的一种类型,目前被认为是门静脉肝窦血管性疾病(porto-sinusoidal vascular disease,PSVD)中合并门静脉高压的一种类型2-3,75%-80% PSVD患者初次就诊常被误诊为“肝硬化”门脉高压症4。本研究旨在评估基于CT图像的机器学习模型鉴别合并门静脉高压的PSVD和肝硬化门静脉高压患者的准确性。
研究方法
本研究纳入了2012年1月至2021年12月期间于首都医科大学附属北京佑安医院按照欧洲血管性肝病兴趣组(VALDIG)和Baveno VII标准诊断为PSVD、且合并门静脉高压的患者2。对照组按1:2的匹配比例纳入同期确诊肝硬化门静脉高压患者。所有患者均行上腹部CT增强扫描。将患者按8:2的比例随机分为训练集和测试集。
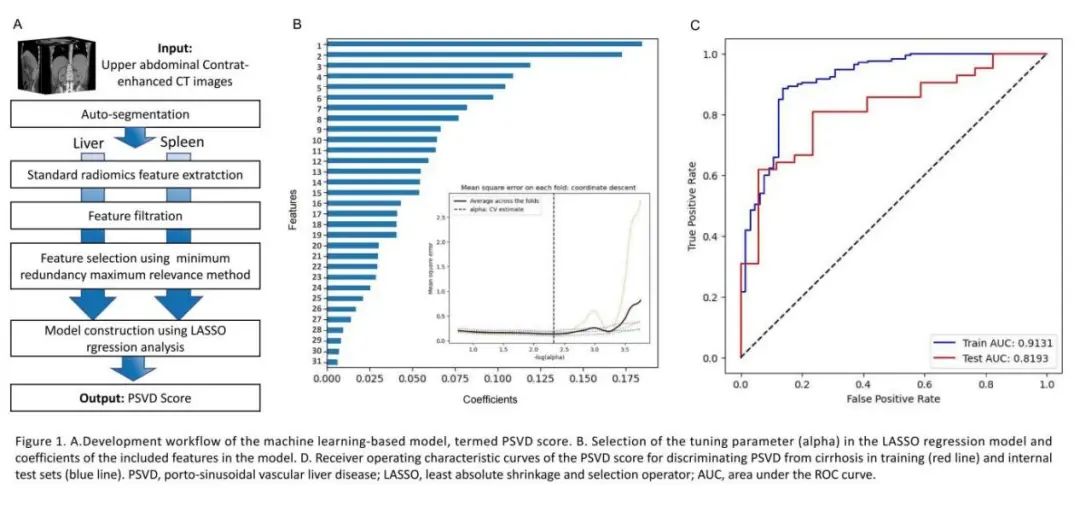
利用机器学习及影像组学技术,在训练集建立了一个基于CT图像的无创诊断模型,称为PSVD评分(图1A)。利用受试者工作特征曲线下面积(area under the receiver operating characteristic curve,AUC)分析模型对鉴别PSVD和肝硬化门静脉高压的准确性,并在内部测试组数据集中验证该模型。
研究结果
本研究共纳入291例患者,其中PSVD 97例,肝硬化194例。按8:2比例随机分组,训练集及测试集样本分别为232例和59例。在训练集中建立PSVD放射组学评分模型,最终纳入31个特征,其中15个来自肝脏,16个来自脾脏(图1B)。PSVD评分具有良好诊断合并门静脉高压PVSD患者的能力,AUC为0.913,在测试组中其诊断准确性进一步得到验证,AUC为0.819(图1C)。
研究结论
基于CT图像的机器学习模型--PSVD评分可较好地鉴别合并门静脉高压的PSVD患者和肝硬化门静脉高压患者。
该研究首次报道了基于CT图像影像组学模型在门静脉高压人群中鉴别PSVD和肝硬化的可行性和准确性5。未来该模型有待在大样本、多中心研究中进行验证,并进一步探索基于影像组学模型的无创评分对PSVD患者预后事件如高危出血风险食管静脉曲张、门静脉血栓形成等的预测效能。
参考文献
1. de Franchis R, Bosch J, Garcia-Tsao G, Reiberger T, Ripoll C. Baveno VII - Renewing consensus in portal hypertension. Journal of Hepatology. 2022; 76:959-74.
2. 徐航飞,丁惠国. 肝(窦)前型非肝硬化门静脉高压症的诊断与治疗及面临的困境. 临床肝胆病杂志, 2019,35(1):13-17.
3. De Gottardi A, Rautou P-E, Schouten J, Rubbia-Brandt L, Leebeek F, Trebicka J, et al. Porto-sinusoidal vascular disease: proposal and description of a novel entity. The Lancet Gastroenterology & Hepatology. 2019; 4:399-411.
4. 张妍,刘晖,丁惠国. 重视非肝硬化门脉高压症的早期诊断. 中国临床新医学, 2021,14(8):745-748.
5. 徐航飞,王宇,何福亮,等. 非肝硬化性门静脉高压食管静脉曲张出血风险的无创评估. 中华肝脏病杂志, 2022,30(10):1092-1099.
(来源:《国际肝病》编辑部)

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
发表评论
全部评论