
编者按
第75届美国肝病研究学会(AASLD)年会于当地时间2024年11月15日—19日在美国圣迭戈隆重召开。首都医科大学附属北京地坛医院谢雯教授团队的3项关于慢性乙型肝炎(CHB)失代偿期肝硬化治疗以及预测CHB合并失代偿期肝硬化患者再代偿的生物学标志物相关研究入选大会壁报,展示了中国学者在这一领域的先进成果,引起广泛关注。《国际肝病》特此报道,以飨读者。
研究一 TAF在治疗失代偿期乙型肝炎肝硬化患者中的疗效与安全性
AASLD 2024壁报展示(No. 4169)
失代偿期肝硬化是CHB的严重并发症,显著增加了肝脏相关疾病发病率和死亡率的风险。TAF(富马酸丙酚替诺福韦)是一种强效抗病毒药物,已显示出优越的安全性特征。然而,关于TAF在治疗CHB合并失代偿期肝硬化患者中的疗效和安全性仍缺乏深入研究。
本回顾性队列研究纳入了2019年1月至2024年2月期间来自4家医院、接受TAF治疗至少96周的CHB合并失代偿期肝硬化患者。在基线时及此后每24周收集包括人口统计学、血液学和影像学信息在内的数据。主要终点是评估第96周时的再代偿率,该再代偿率根据Baveno VII标准定义。次要终点包括评估治疗期间病毒学、血清学和生化参数的变化,以及比较从其他药物转换为TAF治疗的患者与TAF初治患者的疗效。
共纳入235例CHB合并失代偿期肝硬化患者,其中203例完成了96周的观察期。在这些患者中,66例转换为TAF治疗,137例为TAF初治患者。经过96周的抗病毒治疗后,97.5%(198/203)的患者实现了HBV DNA抑制,59.6%(121/203)的患者实现了再代偿。基线时MELD评分较高的患者与基线时MELD评分较低的患者在再代偿率上无显著差异。肝功能检测总体改善,再代偿组的改善程度显著大于非再代偿组(图1)。与转换组相比,TAF初治组的基线HBV DNA水平、ALT、AST(天冬氨酸氨基转移酶)、MELD评分和Child-Pugh评分显著更高。经过96周的治疗后,两组在HBV DNA水平、MELD评分和再代偿率上均无显著差异。
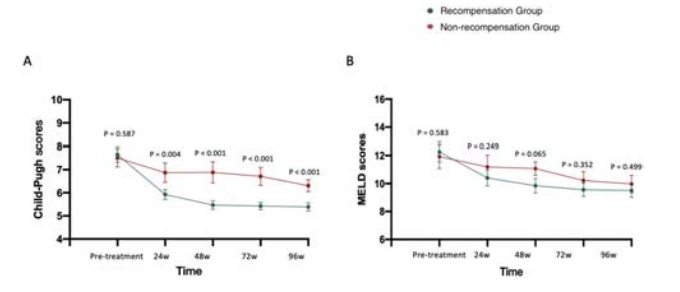
图1. 再代偿组与非再代偿组MELD评分和Child-Pugh评分的变化
研究表明,大多数CHB合并失代偿期肝硬化患者在接受TAF治疗后成功抑制了HBV DNA并改善了肝功能,其中59.6%的患者实现了再代偿。该研究结果提示,无论基线时肝病严重程度如何,TAF都是CHB合并失代偿期肝硬化患者的有效治疗选择。此外,TAF在肾脏和骨骼健康方面也表现出了良好的安全性特征。
研究二 血清N-聚糖作为CHB合并失代偿期肝硬化患者再代偿的预测生物学标志物
AASLD 2024壁报展示(No. 4165)
CHB合并失代偿期肝硬化的患者在治疗后可实现再代偿。然而,预测再代偿仍然具有挑战性。N-聚糖的变化被认为在肝脏疾病中发挥着关键作用。本研究旨在探讨血清N-聚糖对CHB合并失代偿期肝硬化患者再代偿的预测价值。
研究前瞻性入组了接受至少48周抗病毒治疗的CHB合并失代偿期肝硬化患者。再代偿根据Baveno VII标准进行定义。使用GLYFACE®(一种由荧光辅助毛细管电泳提供的专有糖组学分析平台)释放并分析基线血清N-聚糖。选择再代偿组中变化显著(P<0.05)的N-聚糖峰用于建模。基于这些变化,使用逻辑回归分析建立多参数诊断模型。进行受试者工作特征(ROC)曲线分析以评估N-聚糖模型的诊断效能。此外,将多参数诊断模型与临床指标相结合,比较其诊断能力。使用Spearman相关系数评估N-聚糖与临床指标的相关性。
共入组168例患者,平均年龄为52±12岁。其中,75例患者实现再代偿,93例未实现。与未再代偿组相比,再代偿组患者的N-聚糖峰1、2、4和7较低,而峰5较高。此外,再代偿组患者的红细胞(RBC)、血红蛋白(HGB)、血小板(PLT)、ALT、胆碱酯酶(CHE)和HBV DNA水平较高,年龄较小。Spearman相关性分析显示,N-聚糖与凝血酶原时间(PT)、凝血酶原活动度(PTA)、国际标准化比率(INR)、白蛋白(ALB)、球蛋白(GLB)和CHE相关(图2A)。基于N-聚糖的多参数诊断模型预测再代偿的ROC曲线下面积(AUROC)为0.697(图2B)。当与临床指标相结合时,模型的诊断能力提高,AUROC为0.731(图2C)。
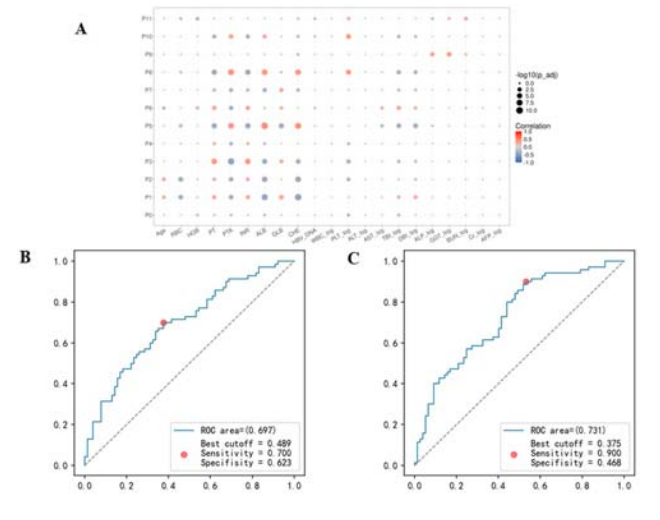
图2. 血清N-聚糖预测的性能和相关性
研究表明,N-聚糖可作为预测CHB合并失代偿期肝硬化患者再代偿的有价值、无创的补充生物学标志物。
研究三 血小板反应蛋白-1作为CHB合并失代偿期肝硬化患者再代偿的预测生物学标志物
AASLD 2024壁报展示(No. 4168)
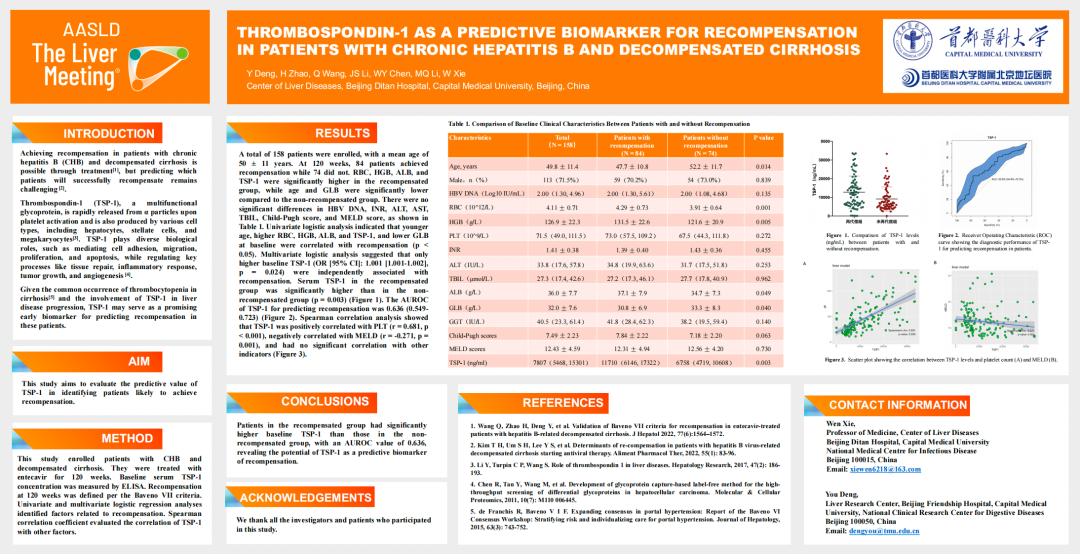
CHB合并失代偿期肝硬化的患者通过治疗有可能实现再代偿,但预测哪些患者能够实现再代偿仍然很困难。血小板减少症是肝硬化患者的常见问题,而血小板反应蛋白-1(TSP-1)与肝病进展有关,这可能为我们提供一些线索。鉴于TSP-1的作用,它有可能成为预测再代偿的早期生物学标志物。本研究旨在评估TSP-1在识别可能实现再代偿的患者中的预测价值。
研究纳入了患有CHB和失代偿期肝硬化的患者,接受恩替卡韦治疗120周。通过酶联免疫吸附试验(ELISA)测定基线血清TSP-1浓度。根据Baveno VII标准定义120周时的再代偿。通过单因素和多因素逻辑回归分析确定与再代偿相关的因素。使用Spearman相关系数评估TSP-1与其他因素的相关性。
共纳入158例患者,平均年龄为50±11岁。在120周时,84例患者实现再代偿,而74例未实现再代偿。再代偿组的RBC、血红蛋白(HGB)、白蛋白(ALB)和TSP-1显著高于未再代偿组,而年龄和GLB显著低于未再代偿组。两组在HBV DNA、INR、ALT、AST、TBIL、Child-Pugh评分和MELD评分方面无显著差异。
单因素逻辑回归分析显示,基线时年龄较小、RBC、HGB、ALB和TSP-1较高以及GLB较低与再代偿相关(P<0.05)。多因素逻辑回归分析表明,只有基线TSP-1较高(OR 1.001;95%CI:1.001-1.002,P=0.024)与再代偿独立相关。再代偿组的血清TSP-1显著高于未再代偿组(P=0.003)(图3A)。TSP-1预测再代偿的AUROC为0.636(0.549-0.723)(图3B)。Spearman相关性分析显示,TSP-1与PLT呈正相关(r=0.681,P<0.001),与MELD评分呈负相关(r=-0.271,P=0.001),与其他指标无显著相关性(图3C)。
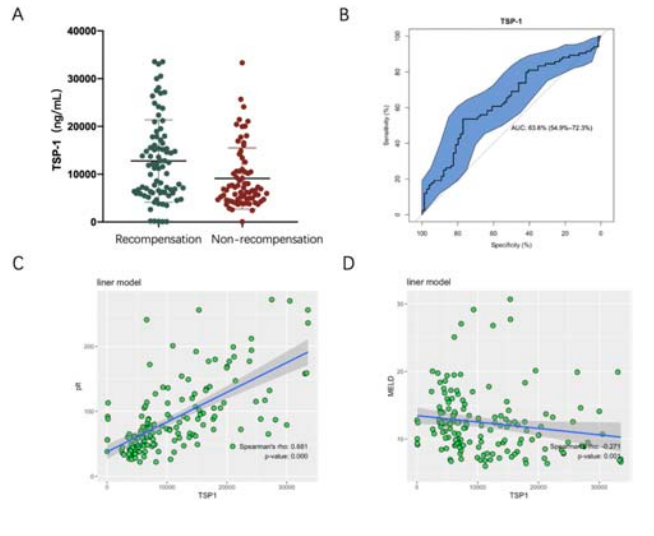
图3. TSP-1预测再代偿的性能与相关性
研究显示,再代偿组患者的基线TSP-1显著高于未再代偿组,TSP-1的AUROC值为0.636,这表明TSP-1有可能成为再代偿的预测生物学标志物。
参考文献
1.1Wen Xie et al. 279 | EFFECTIVENESS AND SAFETY OF TENOFOVIR ALAFENAMIDE IN CHRONIC HEPATITIS B PATIENTS WITH SUBOPTIMAL RESPONSE TO ANTIVIRAL THERAPY
2. Wen Xie et al. 2241 | EFFICACY AND SAFETY OF TENOFOVIR ALAFENAMIDE IN PATIENTS WITH DECOMPENSATED HEPATITIS B CIRRHOSIS
3. Wen Xie et al.2237 | SERUM N-GLYCANS AS PREDICTIVE BIOMARKERS FOR RECOMPENSATION IN PATIENTS WITH CHRONIC HEPATITIS B AND DECOMPENSATED CIRRHOSIS
4. Wen Xie et al. 2240 | THROMBOSPONDIN-1 AS A PREDICTIVE BIOMARKER FOR RECOMPENSATION IN PATIENTS WITH CHRONIC HEPATITIS B AND DECOMPENSATED CIRRHOSIS
(来源:《国际肝病》编辑部)

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
发表评论
全部评论