国际肝病 发表时间:2025/4/11 11:55:24

编者按
3月26日~3月30日,第34届亚太肝病学会年会(APASL 2025)在北京隆重召开,来自世界各地的肝病专家学者共聚一堂分享交流肝病领域最新研究进展。会上,河北医科大学第三医院南月敏教授团队共有15篇研究入选大会口头报告或壁报交流,内容覆盖代谢相关脂肪性肝炎/肝纤维化、病毒性肝炎、药物性肝损伤、胆汁淤积性肝病、肝衰竭、肝细胞癌(HCC)等多领域基础及临床研究。本刊特进行整理报道,供广大同道参考。
专题报告
HBV相关肝细胞癌的一级、二级和三级预防

南月敏教授在报告中着重指出,当前全球肝癌负担形势严峻,HBV依旧是全球范围内导致HCC最常见的病因,全球约42%的HCC病例系由HBV感染所引发。在我国,慢性HBV感染是引发HCC的首要因素,因此,降低HCC发病率的关键在于有效预防与积极治疗HBV感染。研究数据表明,相较于接受规范治疗的患者,未经治疗的HBV感染者每年罹患HCC的风险显著升高。在诸多外源性和内源性危险因素的共同作用下,HBV既可通过直接作用,也能借助间接途径逐步演变为HCC。影响HBV相关HCC患者病情进展的因素众多,涵盖HBV家族史、HCC家族史、HBeAg阴性状态、低病毒血症、谷丙转氨酶(ALT)水平≥40 U/L、肝纤维化、肝硬化以及合并代谢相关脂肪性肝病(MAFLD)等。
为应对这一公共卫生挑战,世界卫生组织(WHO)和中国政府均提出了消除乙型肝炎、提升患者生存率的目标与建议。WHO制定的“到2030年消除病毒性肝炎作为公共卫生威胁”目标明确要求:实现90%的肝炎病毒感染者得到确诊,使新发病毒性肝炎感染病例减少90%,并将病毒性肝炎相关肝硬化和HCC的死亡率降低65%。我国政府在“健康中国2030”规划纲要中亦强调,要加强重大传染病的防控工作,全面推进全民全生命周期的慢性病健康管理,致力于将癌症5年生存率提高15%。
中国近期发布的一系列共识和指南,为HCC的三级预防体系奠定了坚实基础,这些共识和指南不仅为预防、监测、早期发现、早期诊断及采取有效干预措施提供了重要参考,还致力于降低HCC的发病率、预防疾病治愈后的复发、改善患者预后并提高生存率。具体包括:《中国肝癌一级预防策略:专家共识》、《原发性肝癌二级预防共识(2021版)》、《原发性肝癌三级预防共识(2022版)》、《慢性乙型肝炎防治指南(2022年版)》以及《加快消除乙型肝炎病毒感染:扩大预防和治疗的专家建议》等。此外,欧美的相关指南,如AASLD关于HCC预防、诊断、治疗实践指南,EASL关于HCC治疗的临床实践指南,也提供了宝贵的建议。
针对HBV相关HCC的预防措施,具体可分为以下三级:一级预防措施:乙型肝炎疫苗接种。在中国,疫苗接种的广泛推广在降低5岁以下儿童HBV感染率方面发挥了至关重要的作用。二级预防措施:抗病毒治疗。中国、美国及欧洲的指南均一致推荐恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)、丙酚替诺福韦(TAF)及聚乙二醇干扰素(Peg-IFN)作为抗病毒治疗的首选药物。抗病毒治疗显著降低了慢性乙型肝炎患者发生HCC的风险。值得注意的是,慢乙肝患者的低病毒血症状态与终末期肝病及HCC风险的增加密切相关;对于治疗应答不佳或存在低病毒血症的患者,应及时调整治疗方案。三级预防措施:抗病毒治疗同样在HBV相关HCC的三级预防中占据关键地位。多项研究已证实,抗病毒治疗能够显著延长HBV-HCC患者的无进展生存期(PFS)并减少HCC的复发。
口头报告
研究一
中国人群中代谢功能障碍相关脂肪性肝病的肝纤维化非侵入性评估:范围综述(大会编号:OP0136)
研究目的
最新发布的中国指南推荐基于非侵入性检测(NITs)的肝纤维化评估路径,以用于代谢功能障碍相关脂肪性肝病(MAFLD)患者。本综述旨在支持该指南所提出的推荐路径。
研究方法
在六个电子数据库和会议网站中进行了系统性文献检索,时间范围为2012年1月1日至2023年3月7日。纳入使用NITs诊断中国人群肝纤维化的研究,这些研究需以肝活检作为金标准,并报告至少一种诊断性能指标,且论文语言为英文或中文。研究结果采用描述性统计和可视化图表呈现。
研究结果
共纳入79篇研究,涉及469个诊断队列,涵盖四大类共64种不同的NITs。其中,指南推荐的16种成熟NITs在中国人群中表现出良好的诊断性能。此外,还总结了探讨NITs诊断性能影响因素的研究,以及涉及多种NITs联合诊断流程的研究。
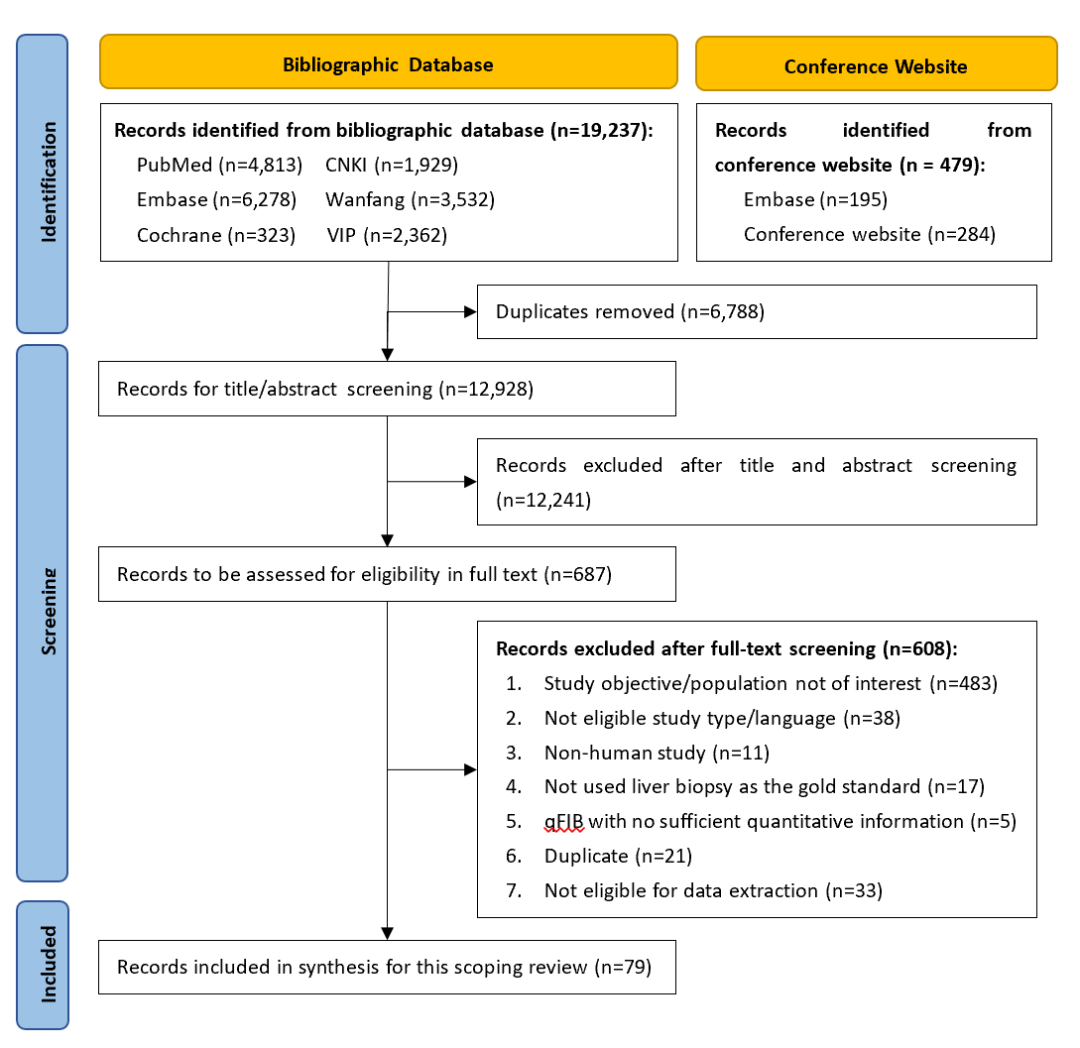
图1. PRISMA(系统评价和荟萃分析首选报告条目)流程图,展示研究筛选过程
(源自APASL 2025会议)
研究结论
本综述提供了充分证据,支持指南推荐的NITs在中国人群中的有效性。然而,瞬时弹性成像(Transient Elastography)的适宜临界值及序贯诊断路径的表现仍需进一步验证。此外,一些在欧美人群中具有潜力的NITs在中国尚缺乏研究。本研究补充了亚洲人群的数据,并可作为亚洲人群的参考。未来研究应重点关注不同临床情境和亚群人群中的临界值分析及报告。
研究二
药物性肝损害严重程度预测模型的建立与评价(大会编号:OP0298)
研究背景
药物性肝损害是临床中常见肝损伤病因之一,重者可导致急性肝衰竭甚至死亡。由于肝脏穿刺活检接受度较低,药物性肝损害目前面临着识别与诊断困难、严重程度及预后难以评估、临床不易管理等挑战。
研究方法
采用回顾性研究,纳入2021.6-2024.10河北医科大学第三医院确诊DILI的125例患者。依据2023年DILI诊疗指南按严重程度分轻度(1级)39例、中重度(≥2级)86例(图2)。用SPSS 27.0.1分析临床数据,行单因素及多因素logistic回归(向后逐步法),并绘ROC曲线。校准曲线、DCA曲线及列线图均由综合性数据分析可视化网络服务平台CNSknowall(https://cnsknowall.com)创建。

图2. 病例筛选与分组
(源自APASL 2025会议)
研究结果
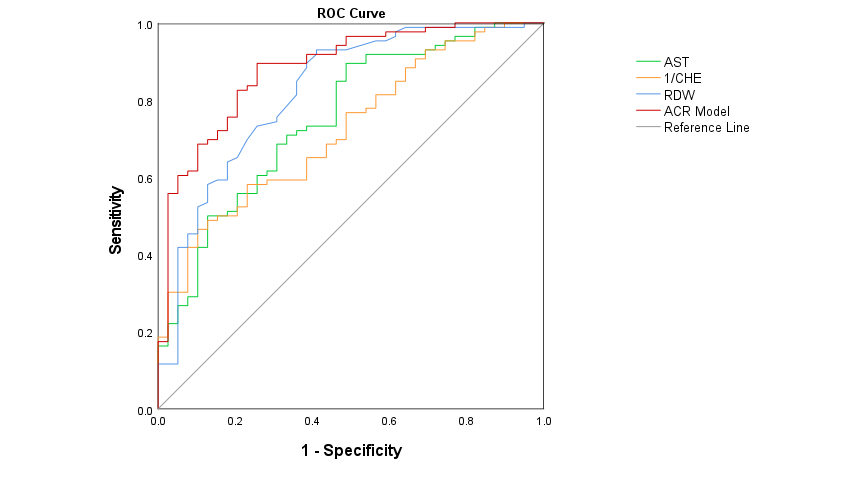
图3. 预测DILI严重程度的AST、CHE、RDW和ACR模型的ROC曲线
(源自APASL 2025会议)
研究结论
ACR模型的预测性能显著优于AST、CHE和RDW。其有望作为评估DILI严重程度的新型预测模型。然而,这些结果仍需在更大规模、多中心的研究中进行验证。
壁报交流
研究三
艾米替诺福韦治疗HBV相关慢加急性肝衰竭患者的短期疗效与安全性分析(大会编号:PP0853)
研究背景
慢加急性肝衰竭(ACLF)病情进展快、预后差,严重影响患者的生活质量。艾米替诺福韦(Tenofovir Amibufenamide,TMF)在慢性乙型肝炎(Chronic Hepatitis B,CHB)和乙型肝炎肝硬化(Cirrhosis)中的疗效和安全性已被证实,但目前仍缺乏TMF治疗HBV-ACLF的真实世界数据。本研究旨在探讨TMF在HBV-ACLF中应用的短期疗效和安全性。
研究方法
本研究回顾性纳入2021.1-2024.10于河北医科大学第三医院就诊的377例HBV-ACLF住院患者,筛选HBV-DNA(+)、抗病毒治疗且生存期>4周者171例。按抗HBV方案分TMF单药组(64例,含TMF、TAF、ETV亚组)和联合组(107例,含TMF+ETV、TAF+ETV、TDF+ETV亚组)(图4)。收集基线、2周、4周时HBV-DNA、肝功、凝血、肾功、电解质、MELD评分等临床数据,用SPSS 26.0以ANOVA和Kruskal-Wallis法分析TMF短期疗效及安全性。
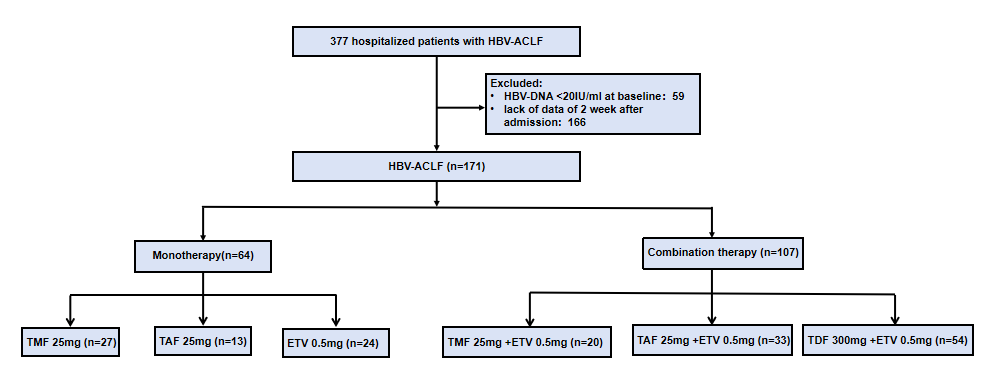
图4. 病例筛选与分组
(源自APASL 2025会议)
研究结果
单药及联合治疗组各亚组患者基线数据组间无统计学差异。
单药治疗:治疗4周,HBV-DNA水平均显著低于基线(TMF、TAF P均<0.001,ETV P=0.006),组间无差异;肝功能、凝血功能改善,TMF组AST治疗2周降幅较TAF、ETV组显著(P<0.05);肾功能(CREA)、骨代谢指标(Ca、P)均正常波动,组间无差异。
联合治疗:治疗2周,TMF+ETV组HBV-DNA降幅虽快于其他组但无统计学差异;治疗4周,三组HBV-DNA均显著低于基线(TMF+ETV、TAF+ETV P均<0.05,TDF+ETV P<0.001),组间无差异;治疗2周和4周,三组肝功能均显著改善(P<0.01),TMF+ETV组、TDF+ETV组PTA显著改善(P<0.01、P<0.001),组间无差异;肾功能和骨代谢指标正常波动,组间无差异。
研究结论
TMF单药或联用ETV治疗HBV-ACLF的疗效、安全性与TAF、ETV单药及TAF/TDF联用ETV等方案相当,为TMF应用提供理论支撑。但研究存在样本量小、随访短、缺乏血脂数据等局限,需开展大规模随机对照试验进一步评估。
研究四
HO-1通过SIRT1/TGF-β/Smad3通路调控代谢相关脂肪性肝病相关肝纤维化的进展(大会编号:PP0837)
研究背景
血红素加氧酶1(HO-1)对由烟酰胺腺嘌呤二核苷酸激活的组蛋白去乙酰化酶Sirtuin 1(SIRT1)具有重要但尚未充分研究的影响,可能通过影响转化生长因子-β(TGF-β)/Smad3通路,进而在非酒精性脂肪性肝病(MAFLD)相关的肝纤维化中发挥作用。本研究旨在阐明HO-1通过SIRT1/TGF-β/Smad3通路调控MAFLD相关肝纤维化的机制。
研究方法
在C57BL/6J小鼠中建立了HO-1诱导和抑制模型,饲喂美硫氨酸和胆碱缺乏(MCD)饮食。此外,野生型小鼠分别饲喂常规饮食或MCD饮食。使用苏木精-伊红、Masson三色染色和Sirius Red染色评估肝脏脂肪变、炎症和纤维化。在体外,通过质粒过表达和小干扰RNA(siRNA)沉默HO-1,处理LX-2细胞。使用细胞计数试剂盒-8(CCK-8)评估细胞活力,通过末端脱氧核苷酸转移酶dUTP标记末端(TUNEL)和免疫荧光法评估细胞凋亡。流式细胞术用于评估细胞凋亡和活性氧(ROS)产生。Western blot和实时定量逆转录聚合酶链反应(RT-qPCR)用于分析与HO-1、SIRT1、TGF-β信号通路及纤维化相关的基因的mRNA和蛋白质表达。
研究结果
饲喂MCD饮食的小鼠出现了显著的肝损伤,包括脂肪变、炎症浸润和细胞周围纤维化(图5)。锌原卟啉治疗加剧了这些病变。与这些结果一致,在LX-2细胞中沉默HO-1可增加纤维化相关基因的表达。此外,HO-1过表达不仅增加了SIRT1的表达,还降低了TGF-β信号通路中关键调控因子的活性,提示HO-1可能与SIRT1/TGF-β通路之间存在潜在的相互作用(图6)。
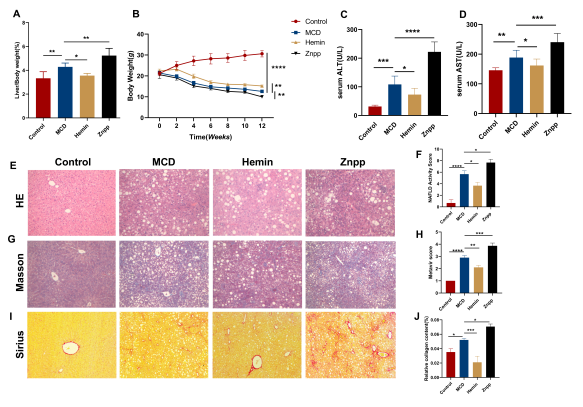
图5. MCD饮食(膳食)的小鼠出现了与脂肪性肝炎相关的肝纤维化
(源自APASL 2025会议)
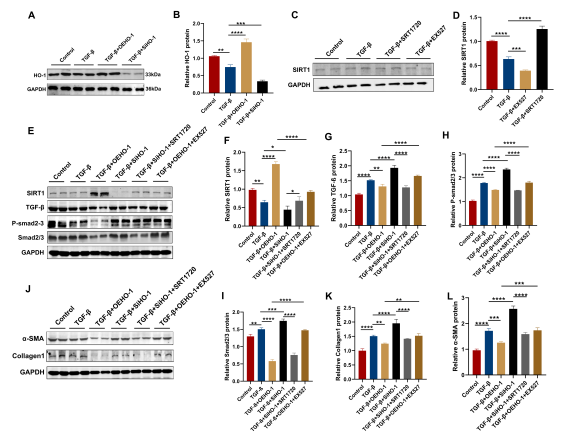
图6. HO-1通过调控SIRT1/TGF-β/Smad3信号通路,在体外介导MAFLD相关的肝纤维化
(源自APASL 2025会议)
研究结论
HO-1通过SIRT1抑制MAFLD相关肝纤维化中的TGF-β/Smad3通路的激活。这些发现为新的治疗策略提供了理论依据。
研究五
新型LPS-A4评分作为慢性乙型肝炎患者肝细胞癌发展的预测模型(大会编号:PP1099)
研究目的
探讨基于iLivTouch的肝硬度测量(liver stiff measurement,LSM)对肝细胞癌(hepatellular carcinoma,HCC)发病率的影响,并建立基于LSM的新型风险模型来预测慢性乙型肝炎(chronic hepatitis B,CHB)患者发生HCC的概率。
研究方法
该回顾性队列研究包括713例患者,并按3:1的比例随机分配到训练组(n = 535)和验证组(n=178)。采用最小绝对收缩和选择算子(LASSO)回归和多变量Cox回归分析优化变量选择。最后,建立HCC发展风险预测模型,通过受试者工作特征曲线、校准图、决策曲线分析对模型进行验证,并进一步进行内部验证。
研究结果
随访期间,训练集和验证集分别有53例(9.9%)和13例(7.3%)患者发生HCC事件。从38个临床特征与实验室指标的变量中,最后筛选到7个变量,用于构建nomogram和预测模型,称为LPS-A4评分。LPS-A4评分包括LSM值、血小板、性别、年龄、饮酒史、白蛋白和乙型肝炎病毒DNA,对预测HCC发展具有良好的准确性,具有相当高的判别性,3年、5年和8年的曲线下的时间依赖面积分别为0.904、0.922和0.921。此外,决策曲线分析显示了良好的临床效益和列线图预测发生风险的实用性。
研究结论
基于LSM的LPS-A4评分为HCC的发展提供了可靠的预测和评估,可能有助于CHB患者的风险分层和早期干预。
研究六
FSP1抑制剂icFSP1通过激活铁死亡使肝细胞癌对Lenvatinib敏感(大会编号:PP1111)
研究目的
Lenvatinib作为晚期肝癌患者的一线靶向治疗药物,其耐药将会导致肿瘤的发展。本研究的主要目的是探讨铁死亡抑制蛋白(FSP1)抑制剂icFSP1与Lenvatinib联合使用时,是否能够提高Lenvatinib对肝癌细胞的敏感性,以期找到更有效的肝细胞癌治疗策略。
研究方法
首先设置空白对照,再根据IC50在肝癌细胞系中加入icFSP1,然后分别使用Lenvatinib单独处理以及Lenvatinib与icFSP1结合处理肝癌细胞。通过对比四组处理方式的肝癌细胞生长曲线、细胞存活率、凋亡率指标,评估icFSP1与Lenvatinib结合使用对肝癌细胞生长和增殖的影响。同时,还检测了肝癌细胞中的铁死亡相关信号蛋白,以探究icFSP1提高Lenvatinib敏感性的可能机制。
研究结果
实验结果显示,与Lenvatinib单独处理相比,Lenvatinib与icFSP1结合处理能够更显著地抑制肝癌细胞的生长和增殖,降低细胞存活率,并促进细胞凋亡(图7)。此外,我们还发现,处理后的细胞铁死亡通路明显激活,这个变化与Lenvatinib敏感性的提高密切相关。具体来说,icFSP1可能通过调节某些关键分子的表达和活性,从而增强Lenvatinib对癌细胞的抑制作用。
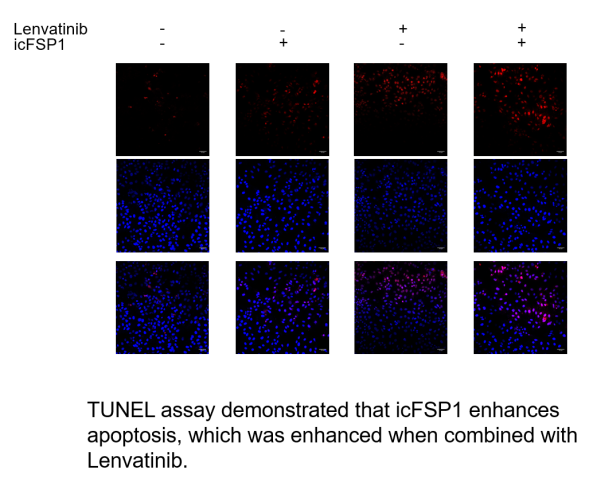
图7. TUNEL实验表明icFSP1 可促进细胞凋亡,与Lenvatinib联用时,icFSP1 的作用加强。
(源自APASL 2025会议)
研究结论
本研究表明,icFSP1与Lenvatinib结合使用能够显著提高Lenvatinib对肝癌细胞的敏感性,从而增强其对癌症的治疗效果。这一发现为癌症治疗提供了新的思路和方法,即通过加入icFSP1,可能能够优化Lenvatinib等激酶抑制剂的治疗效果,为肝细胞癌患者提供更好的治疗方案。未来,我们将继续深入研究icFSP1提高Lenvatinib敏感性的具体机制,并开展更多的临床试验来验证其在实际应用中的效果。
研究七
中药益气活血方通过重塑肠道微生物和改善血清代谢产物治疗代谢相关脂肪性肝炎的研究(大会编号:PP0386)
研究背景
中草药益气活血方(YQHX)是由8种传统中草药组成的复方,临床上被用于治疗代谢相关脂肪性肝炎,但其作用机制尚不明确。我们通过构建小鼠疾病模型结合多组学进一步探讨其分子机制,并尝试对其有效成分进行分析。
研究方法
采用高脂高果糖饮食诱导小鼠代谢相关脂肪性肝炎模型,记录体重、肝比重,留取肠道内容物、血清、肝组织。肝组织病理染色,测血清ALT、肝组织αSMA评估疗效。宏基因测序测肠道菌群,超高效液相色谱串联质谱测血清代谢产物,RNA-seq测肝组织mRNA表达谱,UPLC检测YQHX方有效成分。构建分子-靶点网络筛选关键成分和靶点。体外以棕榈酸诱导AML12细胞模型,经有效成分干预后测细胞活力、脂滴、代谢状态。
研究结果

图8. A 代谢组学分析疾病模型组小鼠和YQHX干预后小鼠的差异代谢产物;B 差异代谢产物之间的相互关系;C 肠道菌群和差异代谢产物的联合分析;D 转录组学分析YQHX治疗后小鼠与疾病模型小鼠的差异基因;E RIPK1/RIPK3/MLKL通路激活引起MAFLD肝细胞发生坏死性凋亡;F YQHX能够重塑肠道微生物和改善血清代谢产物治疗代谢相关脂肪性肝炎
(源自APASL 2025会议)
研究结论
YQHX能够通过重塑肠道菌群和改善代谢产物缓解疾病模型小鼠的代谢相关脂肪性肝炎,所含活性成分芍药苷具有抗坏死性凋亡的作用。这些结果可为进一步的临床研究和开发有效、安全的治疗肝纤维化药物提供一些依据。
研究八/九
CB2受体改善通过改变巨噬细胞表型和YAP/TAZ信号通路改善胆汁淤积性肝纤维化(大会编号:PP0700)
研究背景
肝硬化是各种慢性肝病进展至肝组织以弥漫性纤维化、假小叶形成为特征的病理阶段,其中胆汁淤积是重要病因之一。我们利用胆管结扎(BDL)诱导胆汁淤积肝纤维化小鼠模型,探讨了靶向CB2受体的治疗潜力。
研究方法
使用C57BL/6J 雄性小鼠构建胆管结扎纤维化小鼠模型,将小鼠分为六组,分别为Sham组、Sham+AM1241组、Sham+AM1241溶剂组、BDL组、BDL+AM1241组和BDL+AM1241溶剂组。采用qRT-PCR技术检测各组小鼠肝脏组织 IL - 6、IL - 10、TNF - α、TGF - β、INOS、ARG1、MCP1、MIP1α、MIP2、CD68、CD163、CB2和α - SMA 的 mRNA 水平,采用Western Blot检测各组小鼠肝脏组织YAP、TAZ、CTGF、α - SMA、ARG1、iNOS、CD11b、F4/80和TGF - β 水平。使用 HE、Masson 和 α - SMA 免疫组化等特殊染色评估肝脏纤维化的程度。使用SPSS.21软件进行统计学分析,Adobe IllustratorCS6软件作图,符合正态分布的计量资料采用平均值±标准差表示,多组比较采用单因素方差分析统计学方法;不符合正态分布的计量资料采用中位数和四分位数间距表示,多组比较采用Kruskal-Wallis检验,P<0.05有统计学差异 。
研究结果
小鼠肝组织α-SMA免疫组化染色结果显示,BDL组α-SMA阳性面积明显高于其它组(P<0.05),BDL+AM1241组小鼠α-SMA阳性面积(0.087±0.019)明显小于BDL组小鼠(0.145±0.026)(P<0.05,图9)。
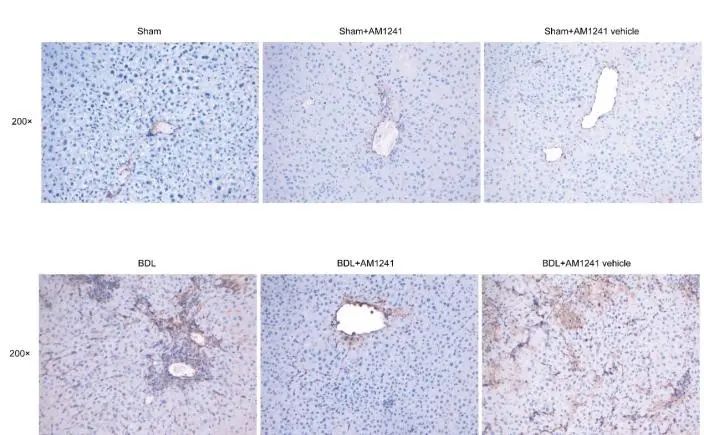
图9. 各组小鼠肝脏组织α-SMA免疫组化(200×)
(源自APASL 2025会议)
qRT-PCR检测结果显示,胆管结扎+AM1241组CB2R表达水平明显高于其它组(P<0.05)。M1相关炎性因子IL-6、TNF-α、INOS、M2相关因子IL-10、TGF-β和纤维化标志物α-SMA的mRNA表达水平均明显低于BDL组小鼠(P<0.05,图10)。
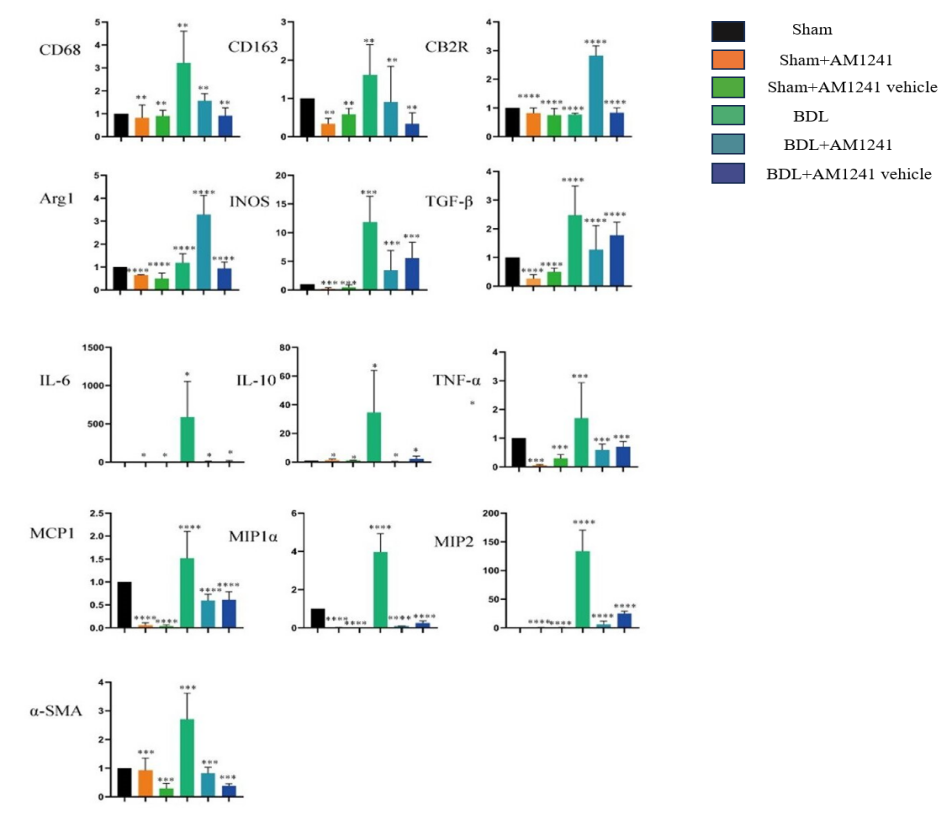
图10. 各组小鼠肝组织匀浆中 Arg1、iNOS、TNF-α、TGF-β、IL-6、IL-10、CD68、CD163、CB2、α-SMA、MCP1、MIP1 和 MIP2 的表达水平
(源自APASL 2025会议)
Western-blot结果显示:在蛋白表达水平上,AM1241可明显减少M1相关炎性因子INOS、F4/80、CD11b,TGF-β,YAP/TAZ通路关键蛋白和纤维化标志物α-SMA、CTGF的表达水平(P<0.05,图11)。
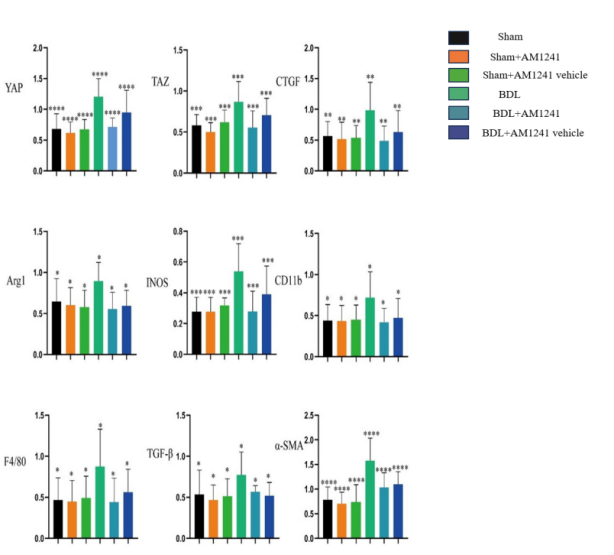
图11. 各组小鼠肝组织匀浆中Arg1、iNOS、CD11b、TGF-β、F4/80、YAP、TAZ、CTGF、α-SMA的表达水平
(源自APASL 2025会议)
研究结论
CB2受体激动剂改善胆汁淤积纤维化反应可能与减少M1相关细胞因子IL-6、TNF-α、INOS,促纤维化因子TGF-β、YAP/TAZ通路关键蛋白的表达有关。
研究十
建立一种快速进展至肝硬化和肿瘤的新型膳食性MASH小鼠模型(大会编号:PP0816)
研究背景
代谢相关脂肪性肝炎(MASH)是非酒精性脂肪性肝病(MAFLD)的最严重表现,已被公认为肝细胞癌(HCC)的主要诱因。然而,MASH-肝纤维化-HCC的分子机制尚不清楚,且目前尚无针对MASH的特异性和有效治疗方法。该领域的研究进展依赖于稳定可靠的临床前模型,以模拟MASH向肝硬化及HCC的持续发展。然而,目前已报道的大多数MASH小鼠模型通常需要超过24周才能发展成MASH,并且其HCC发生率存在不确定性。为克服实验性MASH研究中的这些局限性,我们成功建立了一种具有高度可重复性、普适性和便利性的新型MASH-HCC小鼠模型。
研究方法
本研究使用雄性C57BL/6J小鼠,给予一种新开发的胆碱缺乏和蛋氨酸受限的高脂饮食(OYC-MASH2饮食),持续喂养60周,以观察其肝病进展情况。
研究结果
在喂养OYC-MASH2饮食3周后,小鼠肝脏出现明显的脂肪变性、肝小叶炎症和纤维化,符合MASH的组织学诊断标准。随着喂养时间的延长,所有小鼠在 48 周后均发展为肝硬化。肝脏结节在喂养12周后开始出现,至24周时,所有小鼠的肝脏均形成直径大于2 mm的肿瘤,并在36周后观察到HCC病变的发生。这一模型展现出从MASH到肝硬化及HCC的快速、稳定进展过程,具有较高的实验可重复性。
研究结论
本研究建立了一种进展迅速、高度可重复的MASH-肝硬化-HCC小鼠模型,有助于临床前研究以及探索人类MAFLD-MASH-HCC的发病机制。本模型可为开发针对MASH-HCC的新型治疗药物提供重要的实验基础。
研究十一
IL-24通过促进自噬改善代谢相关脂肪性肝炎(大会编号:EP0311)
研究背景
代谢相关脂肪性肝炎(MASH)患者的自噬通路损伤。目前研究发现 IL-24 是肝脏的保护因素,但在 MASH 疾病中尚未论证,对其通路机制及代谢相关作用也处于未知阶段。本研究根据生物信息学方法成功从246个自噬相关基因筛选出 IL-24 作为 MASH 的关键靶点,探讨IL-24通过mTOR/P70S6K通路对高脂饮食所致MASH的影响,并进一步阐明相关机制。
研究方法
通过喂养高脂饮食建立小鼠MASH模型,鼠尾静脉注射腺相关病毒8体内过表达IL-24;体外用棕榈酸刺激AML12肝细胞模拟脂肪变性,慢病毒感染AML12肝细胞构建体外IL-24过表达模型。自噬双标腺病毒(HBAD-mRFP-GFP-LC3)进一步感染肝细胞,判断细胞自噬流是否通畅。采用免疫组织化学染色和免疫荧光染色观察组织/细胞相关表型变化,Western blot检测自噬相关蛋白p-mTOR/mTOR、 p-P70S6K/ P70S6K、LC3II/LC3I、P62的表达。
研究结果
结果表明IL-24可以改善 MASH小鼠的体重、肝脂肪变性、炎症和纤维化。进一步研究发现,IL-24在体内和体外实验中均能促进自噬通路,增加LC3-II蛋白表达,降低P62蛋白表达。合并应用mTOR抑制剂雷帕霉素可协同IL-24抑制mTOR/P70S6K通路,增强自噬通量(图12)。
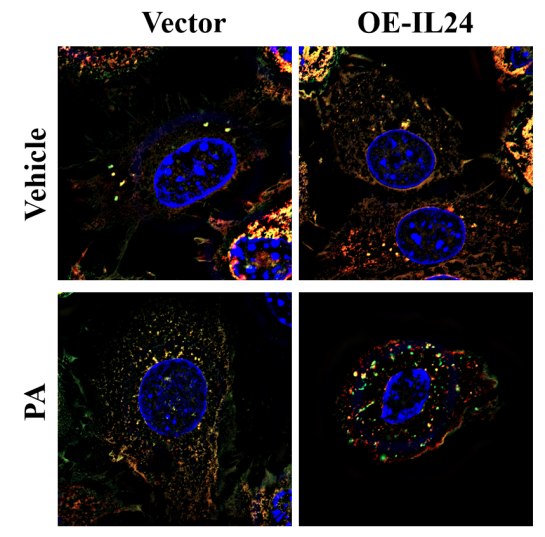
图12. 表达mRFP-GFP-LC3的AML12肝细胞的共聚焦图像,以及PA处理后早期自噬体斑点和自溶体斑点的定量
(源自APASL 2025会议)
研究结论
本研究揭示了IL-24减轻MASH的新机制,即IL-24可能通过抑制mTOR/P70S6K信号通路增强自噬通量。
研究十二
巨噬细胞在人工肝治疗慢加急性肝衰竭中的作用(大会编号:EP0777)
研究目的
人工肝支持系统(ALSS)治疗慢加急性肝衰竭中巨噬细胞相关细胞因子变化的分析及其对肝衰竭患者预后的影响。
研究方法
收集2023年1月至2023年12月在河北医科大学第三医院中西医结合肝病科接受ALSS治疗的ACLF患者28例。根据《肝衰竭诊疗指南》(2018年版)的疗效评判标准将患者分为好转组14例与恶化组14例。留取第一次ALSS治疗前后、最后一次ALSS治疗后抗凝静脉血,用酶联免疫吸附实验试剂盒检测血清中TNF-α、IL-6、IL-10和YAP水平。收集ALSS治疗肝衰竭患者以下指标:第一次ALSS治疗前后、最后一次ALSS治疗后患者血常规、肝肾功能检查、凝血检查、甲胎蛋白等临床检测数据。
研究结果
研究结论
在ACLF患者经ALSS治疗期间,巨噬细胞相关细胞因子水平发生变化,促炎细胞因子水平逐渐降低,抗炎细胞因子水平逐渐升高。IL - 10 和 YAP 水平与改善呈正相关。而HBV相关的ACLF患者,降低sCD163水平有助于患者预后。
研究十三
组织蛋白酶K通过抑制TGF-β1诱导的HSCs激活并促进其凋亡来减轻肝纤维化(大会编号:EP0061)
研究背景
肝纤维化是一种由多种病因引起的复杂伤口愈合反应。肝星状细胞(HSCs)对于肝纤维化的进展至关重要,减少其激活可以减轻纤维化。组织蛋白酶K(CTSK)是一种半胱氨酸蛋白酶,可选择性地切割特定底物,从而调节多个生物过程。已显示CTSK通过抑制成纤维细胞的激活来缓解心脏和肺部的纤维化,但其在肝纤维化中的作用尚不清楚。本研究旨在调查CTSK在肝纤维化中的作用和机制。
研究方法
首先,使用GEO的公开数据集验证CTSK在人类肝纤维化中的表达。此外,通过在培养1天或7天后使用免疫荧光法评估分离的原代小鼠HSCs(pHSCs)中CTSK的表达。使用瞬时和腺病毒转染方法分别研究CTSK过表达对LX2和pHSCs激活和凋亡的影响。使用腺相关病毒血清型8(AAV8)评估CTSK在胆管结扎(BDL)和四氯化碳(CCl4)诱导的肝纤维化小鼠模型中的治疗潜力。
研究结果
高通量分析显示,与正常肝组织相比,纤维化肝活检中的CTSK mRNA水平显著更高;此外,我们发现CTSK表达在纤维化的小鼠肝脏和活化的pHSCs中升高(图13)。数据显示,CTSK的过表达通过调节TGF-β1信号通路抑制了HSCs的激活和增殖,并通过调控凋亡相关蛋白(Bcl-2和Bid)促进了HSCs的凋亡。最后,通过AAV8载体过表达CTSK在CCl4和BDL诱导的小鼠模型中缓解了肝纤维化。
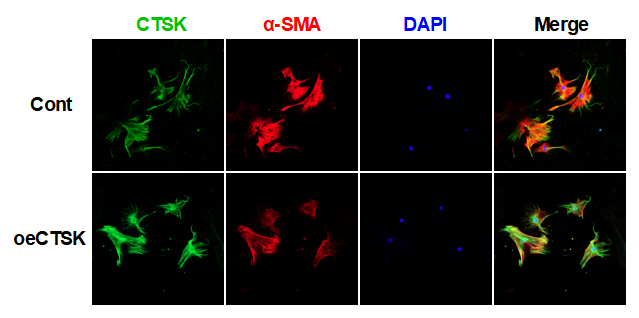
图13. 原代小鼠HSCs中CTSK和α-SMA的双重免疫荧光染色(放大倍数:×100)
(源自APASL 2025会议)
研究结论
我们的研究结果表明,CTSK通过抑制HSCs的激活和增殖,并诱导其凋亡来缓解肝纤维化。CTSK可能是肝纤维化的有希望的治疗靶点。
研究十四
ALKBH1对肝细胞癌的早期诊断及预后评估价值的临床分析(大会编号:EP0912)
研究背景
在中国,肝细胞癌(Hepatocellular carcinoma,HCC)是第五大常见的恶性肿瘤,也是癌症致死的第二大病因,其五年生存率仅为18%。因此,寻找肝癌的新型治疗策略是我们亟待解决的问题。在本研究中,我们检测了ALKBH1在不同的肝细胞癌临床样本中的表达情况,并探究了ALKBH1在肝细胞癌中的诊断效能和预后评估价值。
研究方法
本研究共收集了21对新鲜的肝细胞癌组织及其癌旁组织,以及44对经福尔马林固定、石蜡包埋处理的肝细胞癌组织及其相应的非肿瘤组织。分别采用实时荧光定量聚合酶链式反应(Quantitative Real-Time Reverse Transcription Polymerase Chain Reaction,qRT-PCR)和免疫组织化学法(Immunohistochemistry,IHC)检测ALKBH1的信使核糖核酸(mRNA)和蛋白质表达水平。对65例肝细胞癌患者,评估了ALKBH1表达水平与临床病理特征之间的关联。采用 Kaplan-Meier 分析法比较了不同ALKBH1表达水平的患者之间的无进展生存期(Progression-Free Survival,PFS)。运用 Cox 比例风险回归分析法来确定肝细胞癌患者术后无进展生存期的独立预后因素。
研究结果
与癌旁组织相比,肝细胞癌患者组织及血清中ALKBH1的表达显著升高(P<0.05,图14)。肝细胞癌患者组织中ALKBH1蛋白的表达水平高于非肝细胞癌患者及健康人组织中的表达水平(P<0.05)。病情进展的肝细胞癌患者组织中的ALKBH1水平高于病情未进展的患者(P<0.05,图15)。ALKBH1高表达患者的无进展生存期显著低于ALKBH1低表达的患者。多因素分析表明,ALKBH1高表达、乙肝病毒DNA阳性、血管侵犯以及肿瘤直径大于5cm是肝细胞癌患者术后无进展生存期的独立危险因素(P<0.05)。
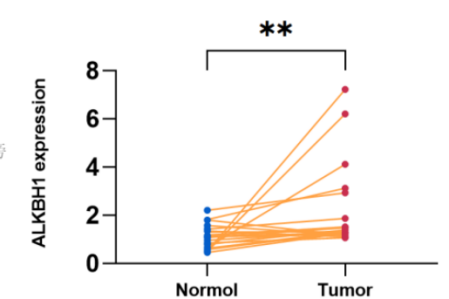
图14. ALKBH1 mRNA在肝细胞癌(HCC)中表达显著升高
(源自APASL 2025会议)
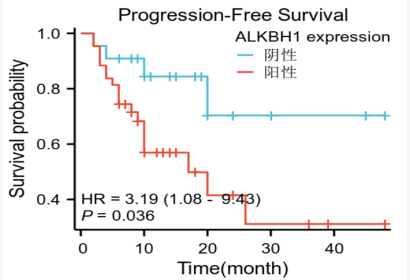
图15. ALKBH1高表达和低表达HCC患者的PFS曲线
(源自APASL 2025会议)
研究结论
ALKBH1在肝细胞癌组织中,无论是在mRNA水平还是蛋白质水平上,均呈现出特异性的过表达,这表明它有潜力成为肝细胞癌恶性表型的分子标志物。ALKBH1的高表达与患者术后无进展生存期的缩短显著相关,并且是肝细胞癌患者术后无进展生存期的一个独立危险因素。ALKBH1有望成为评估肝细胞癌患者术后预后情况的分子标志物。

专家简介

南月敏 教授
河北医科大学第三医院
主任医师,博士生导师
河北医科大学第三医院中西医结合肝病科主任
中华人民共和国政府特殊津贴专家
中华医学会肝病学分会候任主任委员
中华医学会第四届医疗鉴定专家库成员
中国中西医结合医师协会肝病专家委员会副主任委员
中国抗癌协会第二届肿瘤代谢专业委员会副主任委员
主要研究方向:
慢性肝病发病机制、新型诊断技术及临床对策
肝病相关感染的中西医结合诊治
(来源:《国际肝病》编辑部)

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。