国际肝病 发表时间:2025/11/27 21:27:03
编者按:近日,中国人民解放军总医院卢实春教授团队在国际知名跨学科科学期刊Advanced Science(IF 14.1)在线发表了题为《NQO1/p65/CXCL12轴募集的调节性T细胞介导PIVKA-II阳性肝细胞癌对PD-1抑制剂联合仑伐替尼治疗的耐药》的文章。通过临床队列、单细胞RNA测序(scRNA-seq)和实验验证,研究团队系统地探索了肝细胞癌(HCC)中PIVKA-II表达与临床特征和预后的相关性,以及PIVKA-II高表达HCC免疫微环境的改变和对靶免治疗耐药的机制,为克服PIVKA-II高表达患者的免疫治疗耐药性提供了潜在策略方向。高彪博士为本文第一作者。

文章发表封图
HCC是全球癌症死亡的主要原因之一。近年来,随着系统治疗的发展,免疫检查点抑制剂联合抗血管生成药物已成为晚期HCC常用的一线标准治疗方案。相较传统单药治疗,其在客观缓解率(ORR)和长期疗效方面均有明显提升。但临床研究和实践经验提示,仍有一部分患者无法从联合治疗中获益,即存在对免疫联合治疗的原发性耐药。
在肿瘤治疗耐药和进展过程中,由癌细胞、基质细胞、免疫细胞和细胞外基质等组成的肿瘤微环境(TME)起着关键作用,TME特征的改变会对免疫治疗的疗效产生显著影响。而PIVKA-II作为HCC常见的临床诊断生物标志物,虽被证实与不良预后相关,但PIVKA-II高表达HCC患者的TME特征及其对免疫联合治疗的耐药机制,目前仍缺乏充分研究。
研究纳入了2019年1月至2024年6月期间在解放军总医院肝胆胰外科接受治疗的156例手术切除HCC患者;所有患者均未接受过射频消融或免疫治疗等既往治疗,且所有患者均有术前PIVKA-II数据。此外,还收集了104例接受抗PD-1联合仑伐替尼治疗的HCC患者的数据,其中86例患者有治疗前PIVKA-II数据。治疗
对于scRNA-seq,研究者从22例(其中15例接受了一期手术切除,7例在术前接受了抗PD-1联合仑伐替尼治疗)PIVKA-II数据可用的患者中采集了肿瘤组织、癌旁组织和外周血样本,并对另外10例接受抗PD-1联合仑伐替尼治疗的HCC患者的肿瘤组织进行了批量RNA测序以验证结果。此外,研究者收集了17例接受手术切除的HCC患者的配对肿瘤组织和癌旁正常组织,并进行批量RNA测序以作验证。
细胞实验和小鼠肿瘤模型被用于“PIVKA-II高表达患者免疫抑制性TME形成和治疗耐药调控机制”的探索,以及“Plerixafor增强抗PD-1联合仑伐替尼疗效”等研究假设的验证。
01
PIVKA-II高表达与恶性侵袭和对PD-1抑制剂联合仑伐替尼的耐药性相关
为研究PIVKA-II表达与肿瘤侵袭性之间的关联,研究者分析了156例HCC患者的临床数据,并根据PIVKA-II水平(>300 vs. <300 mAU mL-1)进行分层。与PIVKA-II低表达组相比,PIVKA-II高表达组患者表现出更强的侵袭性特征,包括更高的晚期疾病比例、甲胎蛋白(AFP)阳性率、微血管侵犯(MVI)发生率、更大的肿瘤体积以及早期复发率。PIVKA-II高表达组的无进展生存期(PFS)显著缩短(中位PFS:23个月 vs. 53个月)。
图1. PIVKA-II表达与HCC恶性侵袭的关系
(来自Advanced Science)
图2. PIVKA-II表达与PD-1抑制剂联合仑伐替尼治疗疗效的关系
(来自Advanced Science)
02
不同PIVKA-II表达组肿瘤微环境的异质性
对来自15例未经治疗的HCC患者的29个肿瘤/邻近组织样本进行scRNA-seq,结果提示肿瘤组织中T细胞、中性粒细胞和浆细胞浸润减少,而巨噬细胞和基质细胞增加,与免疫冷肿瘤微环境相符。进一步分析揭示了PIVKA-II高表达组和低表达组之间免疫浸润的显著差异:抗肿瘤免疫细胞群(包括细胞毒性T细胞、中性粒细胞、B细胞和树突状细胞)主要富集于PIVKA-II低表达组中,而免疫抑制性巨噬细胞和增殖细胞则在PIVKA-II高表达组中显著升高。多重免疫组化(mIHC)亦证实肿瘤微环境的这种免疫抑制特征。
图3. 不同PIVKA-II表达组肿瘤微环境的异质性
(来自Advanced Science)
注:PLN代表PIVKA-II低表达组临近正常组织,PLT代表PIVKA-II低表达组肿瘤组织,PHN代表PIVKA-II高表达组临近正常组织,PHT代表PIVKA-II高表达组肿瘤组织
值得注意的是,耗竭CD8 T细胞(CD8_PDCD1)和调节性T细胞(Treg)在PIVKA-II高表达组的肿瘤中显著增多,且其浸润水平与血清PIVKA-II水平呈正相关。mIHC亦证实PIVKA-II高表达组中FOXP3+Treg细胞数量增加。此外,来自PIVKA-II高表达组的Treg细胞表现出更高的免疫抑制评分,这与其功能激活相符。
图4. PIVKA-II高表达组肿瘤组织中免疫抑制性T细胞增加
(来自Advanced Science)
在PIVKA-II高表达组肿瘤组织中,肿瘤来源的趋化因子(CCL5、TGFB1)能与Treg受体(CCR4、CCR5、CXCR3)相互作用,促进Treg细胞的募集。而巨噬细胞是该组最富集的免疫细胞类型,在PIVKA-II高表达组中,SPP1+ TAMs浸润显著增加。SPP1+ TAMs参与缺氧、血管生成和炎症相关通路,可能促进血管生成和缺氧微环境的形成,最终促进肿瘤进展。Treg细胞和SPP1+ TAMs两者高度相似的浸润模式,提示其可能共同促进免疫抑制微环境的形成。进一步的NicheNet分析确认,SPP1+ TAMs可通过分泌IL-18、IL-1β和CXCL12等与Treg细胞上的受体相互作用,促进Treg细胞募集和TME中的免疫抑制。
03
PIVKA-II高表达患者免疫抑制性TME形成和治疗耐药的调控机制
在接受抗PD-1联合仑伐替尼治疗的患者中,PIVKA-II高表达组的治疗反应较差,免疫细胞毒性细胞浸润减少,而免疫抑制性巨噬细胞和内皮细胞增多。在无应答患者中,Treg细胞尤其丰富,而细胞毒性CD8+细胞减少。转录组分析表明,无应答患者Treg细胞中免疫抑制基因和增殖基因表达上调,共同支持Treg细胞在治疗耐药中的作用。
HCC细胞是PIVKA-II的主要来源,维生素K循环的破坏会促进PIVKA-II的合成。scRNA-seq数据显示,维生素K循环基因(NQO1、UBIAD1、GGCX、VKORC1、VKORC1L1)在肿瘤细胞中特异性表达。其中,只有NQO1在PIVKA-II高表达的HCC队列和PIVKA-II高表达肿瘤组织中显著上调,提示NQO1上调与HCC驱动的PIVKA-II生成有关。
进一步的细胞实验和小鼠肿瘤模型实验表明,NQO1的上调增强了HCC细胞的迁移和侵袭能力,且通过降低p65的泛素化水平激活NF-κB信号通路并上调CXCL12的表达(注:p65是NF-κB的关键亚基,其泛素化调控NF-κB信号通路的激活;NF-κB二聚体可直接结合CXCL12基因的启动子区域从而启动其转录),而CXCL12在炎症和TME中均发挥着促进Treg细胞募集的关键作用,进一步助力了免疫抑制性TME的形成并导致耐药和肿瘤进展。
图5. NQO1通过抑制p65泛素化激活NF-κB信号通路
(来自Advanced Science)
注:A:NQO1过表达组中TNFA_SIGNALING_VIA_NFKB通路显著富集;B:对照组和NQO1过表达组Huh-7细胞中NF-κB信号通路关键蛋白的表达
04
Plerixafor通过阻断CXCL12介导的Treg细胞募集增强抗PD-1联合仑伐替尼的疗效
体外实验表明,Plerixafor能够抑制CXCL12/CXCR4轴并减少Treg细胞的募集。通过构建小鼠肿瘤模型(包括对照组、NQO1组和NQO1联合Plerixafor治疗组),研究人员发现与NQO1组相比,联合Plerixafor组的肿瘤生长速度显著减慢,肿瘤体积也显著缩小。进一步的流式细胞分析表明:与NQO1组相比,Plerixafor联合治疗组肿瘤组织中CD3+T细胞浸润显著增加,而Treg细胞浸润显著减少。此外,mIHC证实Plerixafor有效降低了Treg细胞的浸润水平。由此,Plerixafor可能通过抑制NQO1介导的Treg细胞浸润来调节肿瘤微环境并抑制肿瘤进展。该假设在NQO1过表达的小鼠HCC模型中得到验证:与其它组相比,NQO1+PD-1抑制剂+仑伐替尼+Plerixafor组的肿瘤体积显著缩小,且疗效更佳。
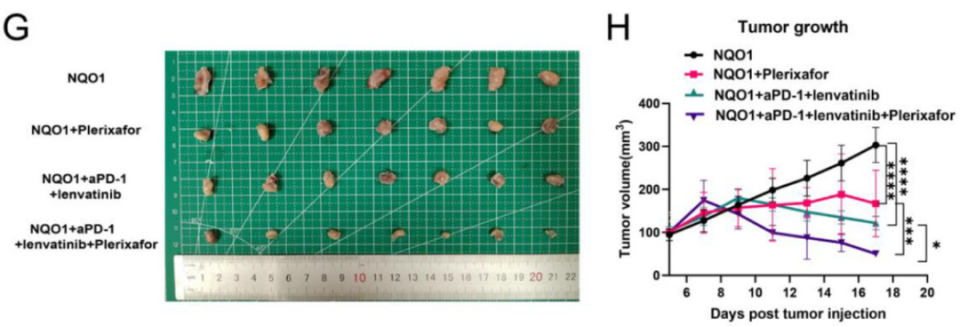
图6. Plerixafor可增强PD-1抑制剂联合仑伐替尼治疗HCC的疗效
(来自Advanced Science)
外周血PIVKA-II水平是预测HCC患者对PD-1抑制剂联合仑伐替尼治疗反应的潜在指标。高PIVKA-II水平与免疫抑制性TME相关,该环境以Treg细胞浸润增加为特征,从而导致治疗耐药。NQO1可通过激活NF-κB促进CXCL12表达,进一步增强Treg细胞的募集。使用Plerixafor阻断CXCL12-CXCR4通路可显著提高治疗效果,为克服高PIVKA-II表达患者的耐药性提供一种有前景的策略。
虽然PIVKA-II是临床批准的HCC诊断生物标志物,但其在肿瘤侵袭性、预后以及对PD-1抗体联合仑伐替尼治疗反应中的作用仍有待明确。通过临床队列分析、scRNA-seq以及细胞和小鼠实验,本研究首次评估了外周血PIVKA-II水平作为治疗反应预测指标的价值,明确了不同PIVKA-II表达组TME的特征,阐释了PIVKA-II高表达患者免疫抑制性TME形成和对PD-1抑制剂联合仑伐替尼治疗耐药的机制,并探索了Plerixafor在阻断CXCL12介导的Treg细胞募集、增强抗PD-1联合仑伐替尼治疗疗效方面的潜在价值。
近年来,在多学科专家的共同推动下,HCC预后改善的探索正不断加速,尤其以免疫为基础的联合治疗为HCC患者带来了令人鼓舞的疗效提升,并为部分疗效响应的患者带来了从“延长生存”到“可能治愈”的希望。然而,治疗耐药仍是当前阻碍很多患者生存获益的重要挑战,本研究的结果为PIVKA-II高表达HCC耐药机制的阐明和临床实践中患者的预后分层提供了新的证据,或将有助于指导HCC的个体化治疗和药物方案调整。
原文链接:Gao B, Wang Y, Sun Z, Tang H, Cao Y, Jiang H, Zhang W, Xu Y, Hu B, Liu Z, Mao G, Li X, Li J, Wan T, Liu B, Zhao X, Jiao S, Li C, Lu S. NQO1/p65/CXCL12 Axis-Recruited Tregs Mediate Resistance to Anti-PD-1 Plus Lenvatinib Therapy in PIVKA-II-Positive Hepatocellular Carcinoma. Adv Sci (Weinh). 2025 Sep 30:e11152. doi: 10.1002/advs.202511152. Epub ahead of print. PMID: 41028931.
专家简介
卢实春 教授
中国人民解放军总医院
主任医师,教授,博士,博士生导师
现任中国人民解放军总医院肝胆胰外科医学部学术主任
中华预防医学会肝胆胰疾病预防与控制专业委员会主任委员
中华医学会器官移植分会第九届委员
北京医学会器官移植分会副主任委员
全军器官移植专业委员会常务委员
中华肝胆外科杂志副总编
中华外科杂志、中华器官移植杂志、中华肝脏病杂志编委
(来源:《国际肝病》编辑部)
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。